题目内容
【题目】Ⅰ.中和滴定
(1)用酸式滴定管量取20.00 mL待测稀盐酸溶液放入锥形瓶中,并滴加1~2滴酚酞作指示剂,用0.20 mol·L-1NaOH标准溶液进行滴定。为了减小实验误差,该同学一共进行了三次实验,假设每次所取稀盐酸体积均为20.00 mL,三次实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗NaOH溶液体积/mL | 19.00 | 23.00 | 23.02 |
该盐酸的浓度约为_____________(保留两位有效数字)。滴定达到终点的标志是_____________。
(2)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______。
A. 滴定终点读数时俯视读数
B. 酸式滴定管使用前,水洗后未用待测盐酸润洗
C. 锥形瓶水洗后未干燥
D. 配制NaOH标准溶液时,没有等溶解液降至室温就转移至容量瓶中
E. 配制NaOH标准溶液时,定容时仰视容量瓶的刻度线
F. 碱式滴定管尖嘴部分有气泡,滴定后消失
Ⅱ.(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是________
A. KMnO4 B. H2O2 C. 氯水 D. HNO3
(2)然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的_______。
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
(3)常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为_______,Fe3+完全沉淀时溶液的pH为________(已知 lg5 = 0.7 )
【答案】0.23 mol·L-1 滴入最后一滴NaOH溶液加入,溶液由无色恰好变成浅红色且半分钟内不褪色 EF B CD 4 3.3
【解析】
Ⅰ.(1)酸遇酚酞不变色,碱遇酚酞变红,利用c(碱)= 来进行计算浓度;(2)根据c(待测)=
来进行计算浓度;(2)根据c(待测)=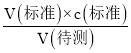 分析不当操作对V(标准)的影响,以此判断浓度的误差;
分析不当操作对V(标准)的影响,以此判断浓度的误差;
Ⅱ.(1)加入合适氧化剂,使Fe2+氧化为Fe3+,不能引入新的杂质;
(2)调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,则加含铜元素的物质与氢离子反应促进铁离子水解转化为沉淀;
(3)依据氢氧化铜饱和溶液中溶度积常数计算溶液中的氢离子浓度,然后计算pH;结合氢氧化铁溶度积和残留在溶液中的离子浓度小于1×10-5 molL-1时就认为沉淀完全。
Ⅰ.(1)利用酸式滴定管量取20.00mL待测稀盐酸溶液放入锥形瓶中,因酸遇酚酞不变色,碱遇酚酞变红,则滴定终点的标志为最后一滴NaOH溶液加入,溶液由无色恰好变成浅红色,半分钟内不褪色;由c(碱)= 可知,因第一次数据差别较大,则V(NaOH)=
可知,因第一次数据差别较大,则V(NaOH)=![]() =23.01mL,则c(HCl)=
=23.01mL,则c(HCl)=![]() ≈0.23 mol·L-1;
≈0.23 mol·L-1;
(2)A.滴定终点读数时俯视读数,读取的标准液的体积偏小,由c(待测)=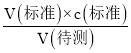 可知测定结果偏低,故A错误;
可知测定结果偏低,故A错误;
B.酸式滴定管水洗后未用待测稀盐酸溶液润洗,盐酸的浓度偏小,所取盐酸溶液的溶质的物质的量偏小,造成V(标准)偏小,根据c(待测)=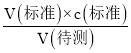 分析,可知测定浓度偏小,故B错误;
分析,可知测定浓度偏小,故B错误;
C.锥形瓶水洗后未干燥,不影响滴定时标准液的体积,根据c(待测)=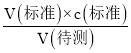 分析,可知测定浓度无影响,故C错误;
分析,可知测定浓度无影响,故C错误;
D.配制NaOH标准溶液时,没有等溶解液降至室温就转移至容量瓶中,配制的标准液浓度偏大,滴定时消耗标准液的体积偏小,由c(待测)=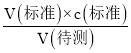 可知测定结果偏低,故D错误;
可知测定结果偏低,故D错误;
E.配制NaOH标准溶液时,定容时仰视容量瓶的刻度线,容量瓶内溶液的体积偏大,导致标准NaOH溶液的浓度偏低,滴定时消耗标准液的体积偏大,由c(待测)=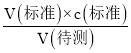 可知测定结果偏高,故E正确;
可知测定结果偏高,故E正确;
F.碱式滴定管尖嘴部分有气泡,滴定后消失,读取的标准NaOH溶液的体积偏大,由c(待测)=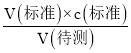 可知测定结果偏高,故F正确;
可知测定结果偏高,故F正确;
故答案为EF;
Ⅱ.(1)加入合适氧化剂,使Fe2+氧化为Fe3+,不能引入新的杂质,A、C、D都会引入杂质,只有过氧化氢的还原产物为水,不引入杂质,故答案为B;
(2)调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,则加含铜元素的物质与氢离子反应促进铁离子水解转化为沉淀,同时不引入新的杂质, NaOH或NH3·H2O会引入Na+或NH4+,而CuO和Cu(OH)2在调节溶液pH的同时不影响溶液的成份,故答案为CD;
(3)Cu(OH)2的溶度积Ksp=3.0×10-20,溶液中CuSO4的浓度为3.0molL-1,c(Cu2+)=3.0molL-1;依据溶度积常数c(Cu2+)×c2(OH-)=3.0×10-20;c2(OH-)=![]() =10-20;得到c(OH-)=10-10mol/L,依据水溶液中的离子积c(H+)×c(OHspan>-)=10-14;可知c(H+)=10-4mol/L,此时溶液pH=4,则Cu(OH)2开始沉淀时溶液的pH为4;残留在溶液中的离子浓度小于1×10-5 molL-1时就认为沉淀完全,Fe(OH)3的溶度积Ksp=8.0×10-38,c(Fe3+)×c3(OH-)=8.0×10-38;c3(OH-)=
=10-20;得到c(OH-)=10-10mol/L,依据水溶液中的离子积c(H+)×c(OHspan>-)=10-14;可知c(H+)=10-4mol/L,此时溶液pH=4,则Cu(OH)2开始沉淀时溶液的pH为4;残留在溶液中的离子浓度小于1×10-5 molL-1时就认为沉淀完全,Fe(OH)3的溶度积Ksp=8.0×10-38,c(Fe3+)×c3(OH-)=8.0×10-38;c3(OH-)=![]() =8.0×10-33;求的c(OH-)=2×10-11mol/L;水溶液中的离子积c(H+)×c(OH-)=10-14;c(H+)=5×10-4mol/L,则pH=3.3。
=8.0×10-33;求的c(OH-)=2×10-11mol/L;水溶液中的离子积c(H+)×c(OH-)=10-14;c(H+)=5×10-4mol/L,则pH=3.3。