��Ŀ����
15��ʵ�飺��0.1mol/LAgNO3��Һ��0.1mol/LNaCl��Һ�������ϵõ���Һ�����ˣ���ȡ�����ٵ���Һ����֧�Թ��У��ֱ�μӵ�Ũ�ȵ������Na2S��Һ��Na2SO4��Һ��ǰ�߳��ֻ��ǣ�������Һ�Գ��壮
��ȡ�����ٵij������μӼ��ΰ�ˮ���������ܽ⣮
���з�������ȷ���ǣ�������
| A�� | ��������AgCl��������Һ��c��Ag+����c��Cl-���������� | |
| B�� | �ٵ���Һ�в�����Ag+ | |
| C�� | �ڵ�����˵�����¶���Ag2S��Ag2SO4������ | |
| D�� | ��������Ag��NH3��2+��ʹc��Ag+����С���ٽ�AgCl��s���ܽ�ƽ�������ƶ� |
���� ��0.1mol/L AgNO3��Һ��0.1mol/L NaCl��Һ�������ϵõ���Һ��˵�������Ȼ���������
�ڷֱ�ȡ�����ٵ���Һ���ֱ�μӵ�Ũ�ȵ�����ı���Na2S��Һ������Na2SO4��Һ��ǰ�߳��ֻ��ǣ�˵���������������Ȼ��������ܵij�����������Һ�Գ��壬˵��δ������������������ʵ��˵���ٹ��˺���Һ����Ȼ���������ӣ�
��ȡ�����Ȼ����������μӼ��ΰ�ˮ���������ܽ⣬˵���˹����������˸��ѵ�������ʣ������������ӣ��ݴ˽�ɣ�
��� �⣺��0.1mol/L AgNO3��Һ��0.1mol/L NaCl��Һ�������ϵõ���Һ��˵�������Ȼ���������
�ڷֱ�ȡ�����ٵ���Һ���ֱ�μӵ�Ũ�ȵ�����ı���Na2S��Һ������Na2SO4��Һ��ǰ�߳��ֻ��ǣ�˵���������������Ȼ��������ܵij�����������Һ�Գ��壬˵��δ������������������ʵ��˵���ٹ��˺���Һ����Ȼ���������ӣ�
��ȡ�����Ȼ����������μӼ��ΰ�ˮ���������ܽ⣬˵���˹����������˸��ѵ�������ʶ����������ӣ�
A��0.1mol/L AgNO3��Һ��0.1mol/L NaCl��Һ�������ϵõ���Һ��˵�������Ȼ�����������Һ��c��Ag+����c��Cl-���������٣���A��ȷ��
B�����ݳ����ܽ�ƽ�⣬�ٵ���Һ�к���Ag+����B����
C�����ݷ�����֪��ǰ�߳��ֻ��ǣ�˵���������������Ȼ��������ܵij�����������Һ�Գ��壬˵��δ������������������C��ȷ��
D����ʵ����Ʋ⣺�������백�����ӵ���ϣ��ٽ����Ȼ������ܽ⣬��D��ȷ��
��ѡB��
���� ���⿼�����ܵ���ʵ��ܽ�ƽ�⼰����ת���ı��ʣ�ע�����ת��Ϊ�ܽ�ȸ�С��������������

| A�� | 1molAl3+���еĺ��������Ϊ3NA | |
| B�� | 0.1L3mol/L���������Һ�к��е�NH4+��ĿΪ0.3NA | |
| C�� | ��״����22.4L������һ������0��HCl���� | |
| D�� | 100mlPH=1�Ĵ�����Һ�к��е�H+����С��0.01NA |
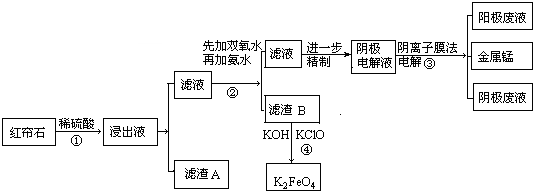
��1����ҵ��Ϊ���ϡ�����ȡЧ��һ���ȡ�Ĵ�ʩ�ǣ�����д���ַ�����
�ٷ������ʯ����߷�Ӧ���¶ȣ�
��2������Һ�е���������H+��Fe2+��Fe3+��Mg2+��Mn2+���������ӷ��ţ�
��3������A����MnO2ԭ��MnO2�����������±���������ԭΪMn2+��
��4����֪��ͬ����������������������������pH���±���
| ���� | Fe3+ | Fe2+ | Mn2+ | Mg2+ |
| ��ʼ������pH | 2.7 | 7.0 | 7.8 | 9.3 |
| ��ȫ������pH | 3.7 | 9.6 | 9.8 | 10.8 |
���̢��мӰ�ˮ������Һ��pH����6��������B�ijɷ�Fe��OH��3��
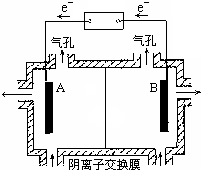
��5�����װ����ͼ��ʾ������Һ���������ƶ��ķ���ΪA��B���A��B����B��A������ʵ�������У�������ϡ����Ϊ���Һ�������ĵ缫��ӦʽΪ2H2O-4e-=O2��+4H+��
��6������B����Ӧ�����ɸ�Чˮ�����������ӷ���ʽ2Fe��OH��3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O��K2FeO4����Ϊ��Чˮ��������ԭ����FeO42-����ǿ�����Կ���ɱ����������ԭ��Fe3+ˮ���Fe��OH��3�����������������ɳ�����
2min��Ӧ�ﵽƽ�⣬����CΪ1.6mol�������з�����ȷ���ǣ�������
| A�� | ����Ӧ��ʼʱ�������Ϊ2 L����v��C��=0.4mol•L-1•min-1 | |
| B�� | ���÷�Ӧ�ں��º����½��У��ų����������� | |
| C�� | ��2 min������������Ͷ������ʵ���A��C����B��ת���ʲ��� | |
| D�� | ���ں�ѹ���������·�Ӧ��ƽ���n��C����1.6mol |
��1��������0.1mol/L��CH3COOH��Һ��ˮϡ���̣����б���ʽ������һ����С����A
A��c��H+������������ ��B��$\frac{c��{H}^{+}��}{c��C{H}_{3}COOH��}$����C��c��H+��•c��OH-���� ��D.$\frac{c��O{H}^{-}��}{c��{H}^{+}��}$
��2��ȡ10mL������Һ������������ˮ������ĵ���ƽ�����ң�����������ҡ��������ƶ�����ȡ10mL������Һ������������ˮ�����ƹ��壨����������ǰ����Һ������ֲ��䣩���������ܽ����Һ��$\frac{c��{H}^{+}��}{c��C{H}_{3}COOH��}$�ı�ֵ����С�����������С������ȷ��������
��3����ͬ�����£�ȡ������ļס�������Һ����ϡ��100����ϡ�ͺ����Һ����pH��С��ϵΪ��pH���ף���pH���ң������������������=������
��4��ȡ������ļס�������Һ���ֱ��õ�Ũ�ȵ�NaOHϡ��Һ��ȫ�кͣ������ĵ�NaOH��Һ�������С��ϵΪ��V���ף���V���ң������������������=������
��5����֪25��ʱ��������ĵ���ƽ�ⳣ�����£�
| ��ѧʽ | ��CH3COOH | ��H2CO3 | ��HClO |
| ����ƽ�ⳣ��K1 | 1.8��10-5 | 4.3��10-7 | 3��10-8 |
| K2 | -- | 5.6��10-11 | -- |
A��HCO${\;}_{3}^{-}$ B��CO${\;}_{3}^{2-}$ C��ClO- D��CH3COO-
д�����з�Ӧ�����ӷ���ʽ��
CH3COOH+NaCO2����������2CH3COOH+CO32-=H2O+CO2��+2CH3COO-��
HClO+Na2CO3����������HClO+CO32-=ClO-+HCO3-��
| A�� | ��ij��Һ�еμ������ữ��Ba��NO3��2��Һ���а�ɫ�������ɣ������Һ��һ������SO42- | |
| B�� | �ñ���NaHCO3��Һ��ȥCO2�����л��е�����SO2 | |
| C�� | ����������������ͨ����������ˮ�ͳ���ʯ��ˮ������ŨH2SO4��ľ̿��Ӧ���ɵ�������� | |
| D�� | ʵ������ȡ������Ϊ�˼ӿ췴Ӧ���ʣ�����ϡ�����еμ�����Cu��NO3��2 |
