题目内容
13.NA为阿伏加德罗常数的值,下列正确的是( )| A. | 1molAl3+含有的核外电子数为3NA | |
| B. | 0.1L3mol/L的硝酸铵溶液中含有的NH4+数目为0.3NA | |
| C. | 标准状况下22.4L盐酸中一定含有0个HCl分子 | |
| D. | 100mlPH=1的醋酸溶液中含有的H+可能小于0.01NA |
分析 A、铝离子的核外有10个电子;
B、铵根离子部分水解,导致溶液中铵根离子数目减少;
C、标况下,盐酸为液态;
D、醋酸是弱电解质,不能完全电离.
解答 解:A、铝离子的核外有10个电子,故1mol铝离子含10mol电子即10NA个,故A错误;
B、.0.1L3mol•L-1的NH4NO3溶液中含有溶质硝酸铵的物质的量为0.3mol,由于铵根离子部分水解,则溶液中含有的铵根离子小于0.3mol,含有的NH4+数目小于0.3NA,故B错误;
C、标况下,盐酸为液态,故不能根据气体摩尔体积来计算其物质的量,故C错误;
D、醋酸是弱电解质,不能完全电离,故溶液中的氢离子的个数小于0.01NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案
相关题目
3.NO和CO都是汽车尾气里的有毒气体,它们能缓慢地反应生成N2和CO2,对此反应下列说法不正确的是( )
| A. | 降低压强能加快反应速率 | B. | 使用适当的催化剂能加快反应速率 | ||
| C. | 改变压强对反应速率无影响 | D. | 温度能加快反应速率 |
1.下列离子反应方程书写正确的是( )
| A. | H2O+H2O═H3O++OH- | |
| B. | CO32-+2H2O?H2CO3+2OH- | |
| C. | Ca(OH)2+2H+?Ca2++2H2O | |
| D. | 2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ |
8.下列说法不正确的是( )
| A. | (CH3)2C=CHCH2CH3的名称为2-甲基-2-戊烯 | |
| B. | 乙醇、乙二醇、丙三醇的沸点依次升高 | |
| C. | 1mol乙酰水杨酸( 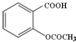 )最多可以和2mol NaOH反应 )最多可以和2mol NaOH反应 | |
| D. | 可用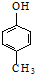 和HCHO 为原料合成 和HCHO 为原料合成 |
18.下列说法不正确的是( )
| A. | 聚乙烯塑料制品可用于食品的包装 | |
| B. | 利用碳酸酯聚合材料生产一次性饭盒可以减少对环境产生的白色污染 | |
| C. | 汽车尾气中的NO、CO等是汽油和柴油的不完全燃烧产物 | |
| D. | 部分烷烃常用于家庭烹饪的燃料气 |
5.现有0.1mol•L-1的醋酸溶液,下列说法正确的是( )
| A. | 加水稀释,溶液中所有离子的浓度都减小 | |
| B. | 溶液中n(CH3COO-)+n(CH3COOH)=0.1mol | |
| C. | 升高温度,醋酸的电离度增大 | |
| D. | 中和1L等物质的量浓度的NaOH溶液所消耗的醋酸体积大于1L |
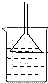
2.关于下列各实验装置的叙述中,不正确的是( )
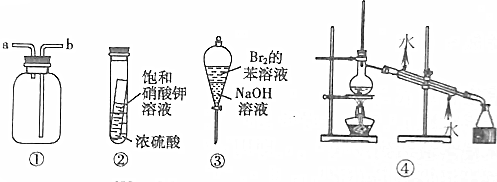

| A. | 装置①可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 | |
| B. | 实验②放置一段时间后,小试管内有晶体析出 | |
| C. | 实验③振荡后静置,上层溶液颜色变浅 | |
| D. | 实验④可用于分离饱和Na2CO3溶液和CH3COOC2H5 |
15.实验:①0.1mol/LAgNO3溶液和0.1mol/LNaCl溶液等体积混合得到浊液,过滤.
②取等量①的滤液于两支试管中,分别滴加等浓度等体积的Na2S溶液、Na2SO4溶液,前者出现浑浊,后者溶液仍澄清.
③取少量①的沉淀,滴加几滴氨水,沉淀逐渐溶解.
下列分析不正确的是( )
②取等量①的滤液于两支试管中,分别滴加等浓度等体积的Na2S溶液、Na2SO4溶液,前者出现浑浊,后者溶液仍澄清.
③取少量①的沉淀,滴加几滴氨水,沉淀逐渐溶解.
下列分析不正确的是( )
| A. | ①中生成AgCl沉淀,溶液中c(Ag+)和c(Cl-)大量减少 | |
| B. | ①的滤液中不含有Ag+ | |
| C. | ②的现象说明该温度下Ag2S比Ag2SO4更难溶 | |
| D. | ③中生成Ag(NH3)2+,使c(Ag+)减小,促进AgCl(s)溶解平衡正向移动 |