题目内容
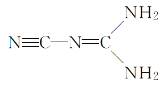
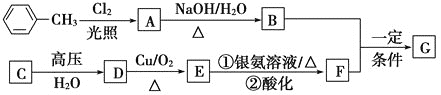
【题目】已知有机物A、B、C、D、E、F、G有如下转化关系,其中C的产量可用来衡量一个国家的石油化工发展水平,G的分子式为![]() ,试回答下列有关问题。
,试回答下列有关问题。
(1)G的结构简式为_________。
(2)指出下列反应的反应类型:A转化为B:________,C转化为D:__________。
(3)写出下列反应的化学方程式
D生成E的化学方程式:___________________。
A生成B的化学方程式:__________________。
(4)符合下列条件的G的同分异构体有________种。
a.苯环上有3个取代基,且有两个取代基相同;
b.能够与新制的银氨溶液反应产生光亮的银镜。
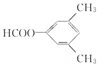
其中共有四种不同化学环境氢原子的同分异构体的结构简式为________、________。
【答案】![]() 取代反应 加成反应 2CH3CH2OH+O2
取代反应 加成反应 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O 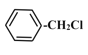 +NaOH
+NaOH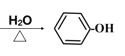 +NaCl 6
+NaCl 6 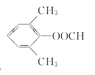
【解析】
C的产量可用来衡量一个国家的石油化工发展水平,则C为CH2=CH2,与水发生加成反应生成D为CH3CH2OH,D发生催化氧化生成E为CH3CHO,E与银氨溶液发生氧化反应生成F为CH3COOH,甲苯与氯气在光照条件发生甲基上的取代反应生成A,A发生水解反应生成B,B与F反应生成G(C9H10O2),由G的分子式可知,B为一元醇,故A为![]() ,B为
,B为![]() ,G为
,G为![]() ,据此解答。
,据此解答。
C的产量可用来衡量一个国家的石油化工发展水平,则C为CH2=CH2,与水发生加成反应生成D为CH3CH2OH,D发生催化氧化生成E为CH3CHO,E与银氨溶液发生氧化反应生成F为CH3COOH,甲苯与氯气在光照条件发生甲基上的取代反应生成A,A发生水解反应生成B,B与F反应生成G(C9H10O2),由G的分子式可知,B为一元醇,故A为![]() ,B为
,B为![]() ,G为
,G为![]() ;
;
(1)由分析可知G的结构简式为![]() ;
;
(2)A转化为B属于水解反应,反应类型为取代反应;C转化为D属于加成反应;
(3)D发生催化氧化生成E为CH3CHO的化学方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O;A发生水解反应生成B的化学方程式为
2CH3CHO+2H2O;A发生水解反应生成B的化学方程式为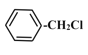 +NaOH
+NaOH +NaCl;
+NaCl;
(4)符合下列条件的![]() 的同分异构体:能够与新制的银氨溶液反应产生光亮的银镜,含有-CHO,苯环上有3个取代基,且有两个取代基相同,还含有2个-CH3,2个-CH3相邻,-CHO有2种位置,2个-CH3处于间位,-CHO有3种位置,2个-CH3处于对位,-CHO有1种位置,故符合条件的同分异构体有2+3+1=6种,其中氢原子共有四种不同环境的所有物质的结构简式为:
的同分异构体:能够与新制的银氨溶液反应产生光亮的银镜,含有-CHO,苯环上有3个取代基,且有两个取代基相同,还含有2个-CH3,2个-CH3相邻,-CHO有2种位置,2个-CH3处于间位,-CHO有3种位置,2个-CH3处于对位,-CHO有1种位置,故符合条件的同分异构体有2+3+1=6种,其中氢原子共有四种不同环境的所有物质的结构简式为: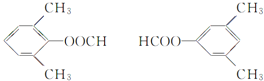 。
。