��Ŀ����
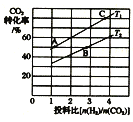
����Ŀ���ǰ�(NH2OH)��ˮ��Һ�еĵ��뷽��ʽΪ��NH2OH+H2O![]() NH3OH++OH-����0.1mol/L����ζ�20mL0.1mol/L NH2OH��Һ���㶨25��ʱ���ζ���������ˮ���������OH-Ũ�ȵĸ���������������Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��
NH3OH++OH-����0.1mol/L����ζ�20mL0.1mol/L NH2OH��Һ���㶨25��ʱ���ζ���������ˮ���������OH-Ũ�ȵĸ���������������Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��
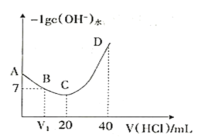
A.A��D��Һ�У�NH2OH���볣������
B.��A��D��ˮ�������c(OH-)��С
C.B���Ӧ����Һ��c(Cl-)=c(NH3OH+)
D.C���Ӧ����Һ��c(H+)=c(OH-)+ c(NH2OH)
���𰸡�B
��������
A. ƽ�ⳣ��ֻ���¶��йأ������¶Ȳ�����볣�����䣬A��ȷ��
B. ��ͼ��֪��C��-lgc(OH-)ֵ��С����ˮ�������c(OH-)���������A��D��ˮ�������c(OH-)�������ټ�С��B����
C. B���Ӧ����Һ�У�-lgc(OH-)=7����ˮ���������c(H+)=c(OH-)=10-7��������Һ�����ԣ�c(H+)=c(OH-)�����ݵ���غ㣺c(NH3OH+) +c(H+)= c(Cl-) +c(OH-)�����c(NH3OH+) = c(Cl-)��C��ȷ��
D. C���Ӧ����Һ�У�������NH2OH��Һǡ����ȫ��Ӧ����ǿ��������NH3OHCl��NH3OHClˮ������NH2OH����Һ�����ԣ����������غ㣺c(Cl-)=(NH3OH+)+c(NH2OH)������غ㣺c(NH3OH+) +c(H+)= c(Cl-) +c(OH-)����ʽ��ӿɵã�c(H+)=c(OH-)+ c(NH2OH)��D��ȷ��
��ѡB��

 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�����Ŀ�����Ž��з���Ƶ�һ��Ԫ��������������������ε��ݱ䣬�����˶�����ʽ��Ԫ�����ڱ������ʾ�Ĺ����ڶ���Ƿ�������Ҫ���á��±���Ԫ�����ڱ��в��ֶ���������Ԫ�ص��й���Ϣ��
Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
T | ������ 5 �ֲ�ͬ�����ĵ��ӣ���������� 2 �ԳɶԵ��� |
X | ����ϼ�Ϊ+7 �� |
Y | ����������Ԫ��ԭ���а뾶��� |
Z | ����������Ӧˮ����������� |
��1����������Ԫ���У�������ӵİ뾶��С����________�������ӷ��ţ���
��2��T �� X ��Ӧ��Ԫ�أ�����̬�⻯���ȶ��Խ�ǿ����_______���ѧʽ����
��3����ԭ�ӽṹ��֪ʶ��˵�� T �� X ��ӦԪ�صķǽ����Ե����ǿ������ T ��ӦԪ�ص���̬�⻯���ˮ��Һ�еμ� X ���ʵ�ˮ��Һ��������_______��д����Ӧ�����ӷ���ʽ _______��
��4��Y �� Z ��ӦԪ�أ�������������Ӧˮ����ɷ�����Ӧ��д���÷�Ӧ�����ӷ���ʽ________��
��5������ Z ��ӦԪ�صĵ��ʣ�����������Ӧ��ұ����������Ӧ��������11.2g���ʣ���ת�Ƶ��ӵ���ĿΪ___��