题目内容
【题目】TiC14是制备钛及其化合物的重要中间体,某小组同学利用下列装置在实验室制备TiCl4,设计实验如下(夹持装置略去):
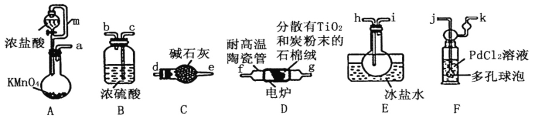
已知:①PdC12溶液捕获CO时,生成金属单质和两种酸性气体化合物。
②

请回答下列问题:
(1)按照气流由左到右的方向,上述装置合理的连接顺序为a→____→____→f→g→___→____→_____→_____→_____(填仪器接口字母)。
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;_____________(按正确的顺序填入下列操作的序号)。
①关闭分液漏斗活塞 ②打开分液漏斗活塞
③停止加热,充分冷却 ④加热装置D中陶瓷管
(3)装置D中除生成TiCl4外,同时生成一种气态不成盐氧化物,该反应的化学方程式为________。
(4)设计实验证明装置E中收集到的液体中含有TiCl4:__________________________。
(5)装置F中发生反应的化学方程式为_____________。用其他方法也可代替装置F,可以是______(写出一种即可)。
(6)制得的TiC14产品中常含有少量CC14,从产品中分离出TiC14的操作名称为_________________。
【答案】c b h i d e j ②④③① TiO2+2C+2Cl2![]() TiCl4+2CO 取少量收集到的液体于洁净试管中,滴加适量水,液体变浑浊,则收集到的液体中含有TiCl4。 PdCl2+CO+H2O=Pd+2HCl+CO2 排水法收集(或用气囊收集等) 蒸馏(或分馏)
TiCl4+2CO 取少量收集到的液体于洁净试管中,滴加适量水,液体变浑浊,则收集到的液体中含有TiCl4。 PdCl2+CO+H2O=Pd+2HCl+CO2 排水法收集(或用气囊收集等) 蒸馏(或分馏)
【解析】
实验装置的顺序一般为发生装置、除杂干燥装置、制备或者发生装置、收集装置、尾气处理装置。TiO2、Cl2和C反应生成TiCl4,根据信息提示PdCl2溶液用于吸收CO,制备的产物中有CO。A装置用于制取Cl2,但是产物TiCl4容易水解,所以Cl2需要干燥,只能用浓硫酸干燥,不能用碱石灰,因为氯气会与碱石灰反应。TiCl4的熔点较低,得到TiCl4的蒸气,E装置用于冷凝得到TiCl4液体。但是尾气中有CO,需要尾气处理,选择F装置,但是需要防止F中的水蒸气进入E中,需要在E和F之间加入干燥管C。因此装置的排序为A、B、D、E、C、F。
(1) A装置用于制取Cl2,但是产物TiCl4容易水解,所以Cl2需要干燥,只能用浓硫酸干燥,不能用碱石灰,因为氯气会与碱石灰反应。TiCl4的熔点较低,得到TiCl4的蒸气,E装置用于冷凝得到TiCl4液体。但是尾气中有CO。CO为有毒气体,需要进行尾气处理,选择F装置,但是需要防止F中的水蒸气进入E中,需要在E和F之间加入干燥管C。因此装置的排序为A、B、D、E、C、F。按照气体流动的顺序为a→c→b→f→g→h→i→d→e→j;
(2)检查装置气密性后,装入药品,TiO2要和Cl2反应,先反应生成Cl2,打开分液漏斗活塞,等装置中充满氯气之后,再加热D中的陶瓷管。等反应完成之后,不能立刻停止氯气的发生。如果先停止生成氯气,再停止加热,装置中的温度下降,压强减小,容易引发倒吸。因此先停止加热,再停止发生氯气。因此顺序为②④③①;
(3)反应物包括TiO2、C、Cl2,生成一种不成盐的氧化物,Ti元素和Cl元素生成TiCl4,那么不成盐的氧化物为C的氧化物CO。根据得失电子守恒,可以写出方程式为TiO2+2C+2Cl2![]() TiCl4+2CO;
TiCl4+2CO;
(4)检验产物中是否为TiCl4,利用TiCl4的性质,根据题中信息可知,TiCl4易水解生成难溶物。答案:取少量收集到的液体于洁净试管中,滴加适量水,液体变浑浊,则收集到的液体中含有TiCl4;
(5)PdCl2用于吸收CO,得到一种金属单质和两种酸性气体。金属单质为Pd,Pd的化合价降低,CO为还原剂,化合物升高,生成CO2,那么另一种酸性气体应该与Cl有关系,为HCl。根据得失电子守恒和原子守恒,方程式为PdCl2+CO+H2O=Pd+2HCl+CO2;F装置用于吸收尾气中的CO气体,用别的装置代替F,也是用于对CO进行尾气处理。可以利用排水法将CO收集起来,也可以利用气囊收集,用燃烧法等方法。答案为排水法收集(或用气囊收集等);
(6)制得的TiC14产品中常含有少量CC14,由于TiCl4易溶于有机溶剂,而且自身也是种液体。对于互溶的液体,可以根据各组分沸点的不同,利用蒸馏法进行分离。答案为蒸馏(或分馏)。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案