��Ŀ����
����Ŀ��25��ʱ��Ksp(AgCl)��1.56��10��10��Ksp(Ag2CrO4)��9.0��10��12������˵����ȷ����(����)
A. ��Ag2CrO4����Һ�м���NaClŨ��Һ��Ag2CrO4������ת��ΪAgCl
B. ��AgCl������Һ�м���NaCl���壬��AgCl��������Һ��c(Cl��)��c(Ag��)
C. AgCl��Ag2CrO4���������Һ�У�![]() ��
��![]()
D. ��ͬŨ�ȵ�Na2CrO4��NaCl�����Һ�еμ�AgNO3��Һ��AgCl������
���𰸡�D
��������Ag2CrO4�ܽ�ȴ���AgCl�����������������������ת�������ƣ���![]() Ag2CrO4��ת��ΪAgCl����A������AgCl������Һ�м���NaCl���壬����AgCl����������c��Ag+����c��Cl-��=1.56��10-10����c��Cl-����c��Ag+������B�������߹������Һ�У����ڣ�Ksp��AgCl��=c��Ag+����c��Cl-��=1.56��10-10��Ksp��Ag2CrO4��=c2��Ag+����c��CrO42-��=9.0��10-12����
Ag2CrO4��ת��ΪAgCl����A������AgCl������Һ�м���NaCl���壬����AgCl����������c��Ag+����c��Cl-��=1.56��10-10����c��Cl-����c��Ag+������B�������߹������Һ�У����ڣ�Ksp��AgCl��=c��Ag+����c��Cl-��=1.56��10-10��Ksp��Ag2CrO4��=c2��Ag+����c��CrO42-��=9.0��10-12����![]() =
=![]() ����C������������ʱ��AgCl��Һ��c��Ag+��=
����C������������ʱ��AgCl��Һ��c��Ag+��=![]() ��Ag2CrO4��Һ��c��Ag+��=
��Ag2CrO4��Һ��c��Ag+��=![]() ��ͬŨ�ȵ�Na2CrO4��NaCl���ݴ˵ó����ߴ���ǰ�ߣ�c��Ag+��ԽС����Խ�����ɳ����������������Ӳ����������Ⱥ�˳��ΪCl-��CrO42-����D��ȷ��
��ͬŨ�ȵ�Na2CrO4��NaCl���ݴ˵ó����ߴ���ǰ�ߣ�c��Ag+��ԽС����Խ�����ɳ����������������Ӳ����������Ⱥ�˳��ΪCl-��CrO42-����D��ȷ��

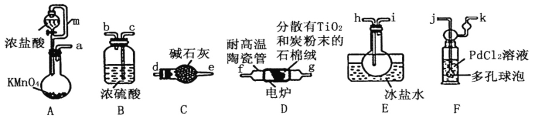
����Ŀ��ʵ����Ϊ̽������Ũ����(����)�ķ�Ӧ������֤SO2�����ʣ������ͼ��ʾװ�ý���ʵ�飬����˵������ȷ����( )

A��װ��B������KMnO4��Һ����ɫ�������˶�������Ļ�ԭ�� |
B��ʵ����������װ��A����Һ�еμ�KSCN��Һ�Լ������ɵ�Fe3+ |
C��װ��D��Ʒ����Һ��ɫ������֤SO2��Ư���� |
D��ʵ��ʱ������a����Ũ�����У��ɷ�ֹװ��B�е���Һ���� |