题目内容
【题目】(1)反应3Fe(S)+4H2O(g)=Fe3O4(s)+4H2(g)在一可变的容积的密闭容器中进行,试回答:
①增加Fe的量,其正反应速率的变化是_______(填增大、不变、减小,以下相同)
②将容器的体积缩小一半,其正反应速率________
③保持体积不变,充入N2使体系压强增大,其正反应速率________。
④保持压强不变,充入N2使容器的体积增大,其正反应速率_______。
(2)将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:
3A(g)+B(g) xC(g)+2D(g),5 min后测得c(D)=0.5 mol·L-1,c(A)∶c(B)=3∶5,C的反应速率是0.1 mol·L-1·min-1。
①A在5 min末的浓度是___________。② v(B) =___________。 ③ x=_______。
【答案】不变 增大 不变 减小 0.75 mol·L-1 0.05 mol·L-1·min-1 2
【解析】
(1)①因铁是固体,增加铁的量,不能增加铁的浓度,不能改变反应速率,故答案为:不变;
②容器的体积缩小,容器内各气体的浓度都增大,浓度越大,化学反应速率越快,故答案为:增大;.
③体积不变,充入N2使体系压强增大,但各气体的浓度不变,反应速率不变,故答案为:不变;
④压强不变,充入N2使容器的体积增大,但各气体的浓度都减小,浓度越小,反应速率越小,故答案为:减小;
(2)①平衡时D的浓度为0.5mol·L-1,D的物质的量为2L×0.5mol·L-1=1mol,则:
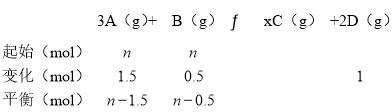
所以(n-1.5):(n-0.5)=3:5,解得n=3,
A在5min末的浓度是![]() =0.75 mol·L-1,故答案为:0.75mol·L-1;
=0.75 mol·L-1,故答案为:0.75mol·L-1;
②从开始到平衡时B的平均反应速率=![]() =0.05 mol·L-1·min-1 ,故答案为:0.05 mol·L-1·min-1 ;
=0.05 mol·L-1·min-1 ,故答案为:0.05 mol·L-1·min-1 ;
③反应速率之比等于化学计量数之比,所以v(B):v(C)=0.05mol·L-1·min-1 :0.1mol·L-1·min-1 =1:x,所以x=2,故答案为:2。

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案【题目】向如图所示的装置中缓慢地通入气体X,若关闭活塞K,则品红溶液无变化而澄清石灰水变浑浊:若打开活塞K,则品红溶液褪色.X和Y可能是

A | B | C | D | |
X | NO2 | SO2 | HCl | Cl2 |
Y | 饱和NaOH溶液 | 饱和碳酸氢钠溶液 | 亚硫酸钠溶液 | 亚硫酸钠溶液 |
A.AB.BC.CD.D