题目内容
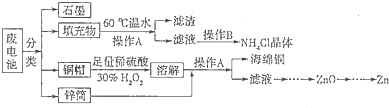
某电化学实验装置如图所示,下列说法正确的是


| A.若X为碳棒,开关K置于M处,则溶液中的H+移向Fe极 |
| B.若X为碳棒,开关K置于N处,转移0.2mole一时析出0.lmolO2 |
| C.若X为铜棒,开关K置于M或N处,均可减缓铁的腐蚀 |
| D.若X为锌棒,开关K置于M或N处,锌电极上反应均为Zn-2e一=Zn2+ |
D
试题分析:A.若X为碳棒,开关K置于M处,则装置是原电池,Fe是负极,C作正极,根据同种电荷相互排斥,异种电荷相互吸引的原则,溶液中的H+移向负电荷较多的正极C棒。错误。 B.若X为碳棒,开关K置于N处,该装置为电解池,转移0.2mole一时析出0.05molO2。错误。 C.若X为铜棒,开关K置于M处,Fe、Cu及硫酸构成原电池,Fe作负极,可以加快铁的腐蚀;若开关K置于N处,Cu为阳极,发生反应失去电子,而Fe作阴极而被保护,因此可减缓铁的腐蚀。错误。D.若X为锌棒,开关K置于M处,构成的是Zn、Fe原电池,Zn的活动性比Fe强,所以锌电极上反应为Zn-2e一=Zn2+;当或开关K置于N处,该装置为电解池,Zn是阳极,是活性电极,发生反应Zn-2e一=Zn2+;正确。

练习册系列答案
相关题目



 是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题: