题目内容
16.下列说法正确的是( )| A. | 酸式盐的水溶液一定显碱性 | |
| B. | 只要酸和碱的物质的量浓度和体积分别相等,它们反应后的溶液就呈中性 | |
| C. | 纯水呈中性是因为水中氢离子的物质的量浓度和氢氧根离子的物质的量浓度相等 | |
| D. | 碳酸溶液中氢离子的物质的量浓度是碳酸根离子的物质的量浓度的2倍 |
分析 A、弱酸的酸式盐存在电离和水解,溶液酸碱性取决于电离程度和水解程度大小;
B、酸碱强弱不同,元数不同酸碱性不同;
C、中性溶液中氢离子的浓度等于氢氧根离子的浓度;
D、碳酸是弱酸部分电离.
解答 解:A、弱酸的酸式盐存在电离和水解,溶液酸碱性取决于电离程度和水解程度大小,若NaHSO3溶液呈酸性,NaHCO3溶液呈碱性,故A错误;
B、酸碱强弱不同,元数不同酸碱性不同,如醋酸和氢氧化钠反应生成醋酸钠溶液显碱性,故B错误;
C、中性溶液中氢离子的浓度等于氢氧根离子的浓度,所以纯水呈中性是因为水中氢离子的物质的量浓度和氢氧根离子的物质的量浓度相等,故C正确;
D、碳酸是弱酸部分电离,电离方程式为H2CO3  H++HCO3-,HCO3-
H++HCO3-,HCO3- H++CO32-以第一步电离为主,则氢离子浓度大于碳酸根离子浓度的2倍,故D错误;
H++CO32-以第一步电离为主,则氢离子浓度大于碳酸根离子浓度的2倍,故D错误;
故选C.
点评 本题考查了盐类水解和弱酸的电离的分析判断,溶液酸碱性的理解应用,掌握基础是关键,题目较简单,注意酸式盐溶液的酸碱性的判断.

练习册系列答案
相关题目
4.Ⅰ.已知25℃时有关弱酸的电离平衡常数:
(1)25℃时,将20mL 0.1mol/LCH3COOH溶液和20mL0.1mol/LHSCN溶液分别与20mL 0.1mol/LNaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图1所示:
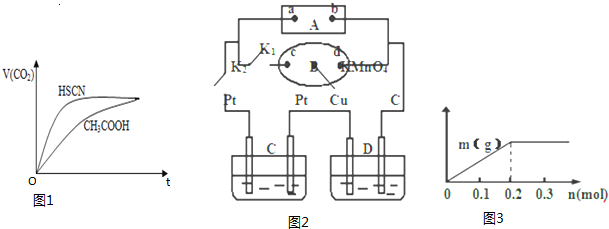
反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是相同温度下HSCN比CH3COOH的电离平衡常数大,同浓度时电离出的氢离子浓度大,与NaHCO3溶液反应快
(2)若保温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是b(填序号).
a.c(CH3COO-) b.c(H+) c.Kwd.醋酸电离平衡常数
Ⅱ.某温度(t℃)时,测得0.01mol/L的NaOH溶液的pH=11.在此温度下,将pH=2的H2SO4溶液VaL与pH=12的NaOH溶液VbL混合,若所得混合液为中性,则Va:Vb=10:1.
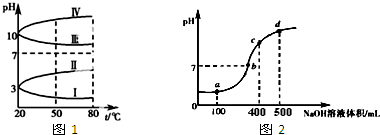
Ⅲ.如图2所示,A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液均见图示.
(1)关闭K1,打开K2,通电后,B的KMnO4紫红色液滴向c端移动,则电源b端为负极,通电开始时,滤纸d端的电极反应式是2H++2e-=H2↑.
(2)已知C装置中溶液为Cu(NO3)2和X(NO3)3,且均为0.1mol,打开K1,关闭K2,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图3所示.则Cu2+、X3+、H+氧化能力由大到小的顺序是Cu2+>H+>X3+;D装置中溶液是H2SO4,则此装置电极C端的实验现象是在C端开始时有无色无味气体产生,一段时间后有红色物质析出.
| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |

反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是相同温度下HSCN比CH3COOH的电离平衡常数大,同浓度时电离出的氢离子浓度大,与NaHCO3溶液反应快
(2)若保温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是b(填序号).
a.c(CH3COO-) b.c(H+) c.Kwd.醋酸电离平衡常数
Ⅱ.某温度(t℃)时,测得0.01mol/L的NaOH溶液的pH=11.在此温度下,将pH=2的H2SO4溶液VaL与pH=12的NaOH溶液VbL混合,若所得混合液为中性,则Va:Vb=10:1.
Ⅲ.如图2所示,A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液均见图示.
(1)关闭K1,打开K2,通电后,B的KMnO4紫红色液滴向c端移动,则电源b端为负极,通电开始时,滤纸d端的电极反应式是2H++2e-=H2↑.
(2)已知C装置中溶液为Cu(NO3)2和X(NO3)3,且均为0.1mol,打开K1,关闭K2,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图3所示.则Cu2+、X3+、H+氧化能力由大到小的顺序是Cu2+>H+>X3+;D装置中溶液是H2SO4,则此装置电极C端的实验现象是在C端开始时有无色无味气体产生,一段时间后有红色物质析出.
11.X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
(1)W位于元素周期表第三周期第ⅣA族;W的原子半径比X的大(填“大”或“小”).
(2)Z的第一电离能比W的小(填“大”或“小”); XY2由固态变为气态所需克服的微粒间作用力是分子间作用力;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称CH3CH2OH、CH3COOH等.
(3)W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是Si+4HF=SiF4↑+2H2↑.
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
(2)Z的第一电离能比W的小(填“大”或“小”); XY2由固态变为气态所需克服的微粒间作用力是分子间作用力;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称CH3CH2OH、CH3COOH等.
(3)W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是Si+4HF=SiF4↑+2H2↑.
8.已知2SO2(g)+O2(g)?2SO3(g).若在500℃和催化剂的作用下,该反应在容积固定的密闭容器中进行,下列有关说法不正确的是( )
| A. | 升高温度,可以加快反应速率 | |
| B. | 使用催化剂是为了加快反应速率 | |
| C. | 在上述条件下,SO2不能完全转化为SO3 | |
| D. | 达到平衡时,SO2的浓度与SO3的浓度一定相等 |
5.关于反应中的先后顺序,下列评价正确的是( )
| A. | 向浓度都为0.1mol•L-1Na2CO3和NaOH混合溶液中通入CO2,NaOH首先反应 | |
| B. | 向NH4Al(SO4)2溶液中滴加少量的NaOH溶液,NH4+首先反应 | |
| C. | 向浓度都为0.1mol•L-1的FeCl3和CuCl2混合溶液中加入铁粉,CuCl2首先反应 | |
| D. | 向0.1mol•L-1的FeCl3溶液中加入质量相同、颗粒大小相同的铁和铜,铜首先反应 |
6.25℃时,H2SO3及其钠盐的溶液中,H2SO3、HSO3-、SO32-的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是( )
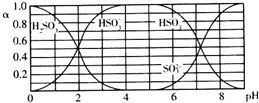

| A. | 溶液的pH=5时,硫元素的主要存在形式为HSO3- | |
| B. | 当溶液恰好呈中性时:c(Na+)>c(SO32-)+c(HSO3-) | |
| C. | 向pH=8的上述溶液中滴加少量澄清石灰水,$\frac{{c({HSO_3^-})}}{{c({SO_3^{2-}})}}$的值增大 | |
| D. | 向pH=3的上述溶液中滴加少量稀硫酸,α(HSO3-)减小 |
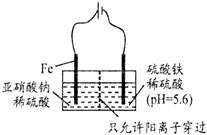 利用15N可以测定亚硝酸盐对地下水质的污染情况.
利用15N可以测定亚硝酸盐对地下水质的污染情况. ,15N2的结构式为15N≡15N;
,15N2的结构式为15N≡15N;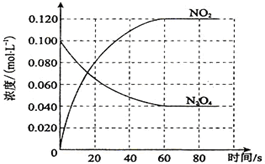 在容积为100L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2 (g),随温度升高,混合气体的颜色变深.反应的△H大于0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如图所示.在0~60s时段,反应速率v(N2O4)为0.0010mol/(L•s).
在容积为100L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2 (g),随温度升高,混合气体的颜色变深.反应的△H大于0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如图所示.在0~60s时段,反应速率v(N2O4)为0.0010mol/(L•s).