题目内容
向甲、乙两个容积均为1 L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2(其中,甲充入2 mol SO2、1 mol O2,乙充入1 mol SO2、0.5 mol O2),发生反应:2SO2(g)+O2(g)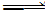 2SO3(g);ΔH=-197.74 kJ·mol-1。
2SO3(g);ΔH=-197.74 kJ·mol-1。
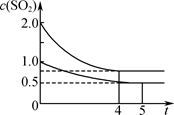
一段时间后达到平衡,测得两容器中c(SO2)(mol·L-1)随时间t(min)的变化关系如右图所示。下列说法正确的是( )
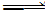 2SO3(g);ΔH=-197.74 kJ·mol-1。
2SO3(g);ΔH=-197.74 kJ·mol-1。
一段时间后达到平衡,测得两容器中c(SO2)(mol·L-1)随时间t(min)的变化关系如右图所示。下列说法正确的是( )
| A.热量:Q(甲)<2Q(乙) |
| B.压强:p(甲)<2p(乙) |
| C.乙中前5 min内的反应速率v(O2)=0.10 mol·L-1·min-1 |
| D.保持其他条件不变,若起始时向乙中充入0.4 mol SO2、0.2 mol O2、0.4 mol SO3,则此时v(正)<v(逆) |
BD
试题分析:A、两容器反应若为等效平衡,则产生的热量Q(甲)=2Q(乙),但容器乙中物质的量少,压强低平衡逆向移动,产生的热量少,故有Q(甲)>2Q(乙),错误;B、同A,相对于甲容器,乙容器压强低,平衡逆向移动,气体总物质的量变多,压强变大,正确;C、乙中前5 min内的反应速率v(O2)=1/2v(SO2)=0.05mol·L-1·min-1,错误;
2SO2(g)+O2(g)
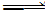 2SO3(g)
2SO3(g)始量 1 0.5 0
转化量 0.5 0.25 0.5
平衡量 0.5 0.25 0.5
该反应的平衡常数k=0.52÷(0.52×0.25)=4
此时Q=0.42÷(0.42×0.2)=5>k,平衡逆向移动,正确。

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
 bB(g)达平衡后,保持温度不变,将容器容积增加一倍,达到新平衡时,B的浓度是原来的60%。则下列叙述正确的是( )
bB(g)达平衡后,保持温度不变,将容器容积增加一倍,达到新平衡时,B的浓度是原来的60%。则下列叙述正确的是( ) B(g)+c(g),在其他条件不变的情况下,再充入一定量的A气体,A的转化率将增大
B(g)+c(g),在其他条件不变的情况下,再充入一定量的A气体,A的转化率将增大
 2SO3 ΔH< 0 ,达平衡后,增大压强
2SO3 ΔH< 0 ,达平衡后,增大压强 2C(气)达到平衡的标志是
2C(气)达到平衡的标志是 Fe(s) + H2O,K=0.52。欲使容器中有1.0 mol FeO被还原,反应前容器中应充入a mol H2。则a最接近
Fe(s) + H2O,K=0.52。欲使容器中有1.0 mol FeO被还原,反应前容器中应充入a mol H2。则a最接近 2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表: 2CO(g)+2H2(g) 的△H= ;
2CO(g)+2H2(g) 的△H= ;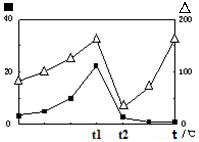 (?代表CO的生成速率,■代表催化剂的催化效率)
(?代表CO的生成速率,■代表催化剂的催化效率)