题目内容
16.研究表明,Na2FeO4是一种高效多功能水处理剂,应用前景广阔,可用FeSO4和Na2O2反应制备,在反应中.FeSO4与Na2O2的物质的量之比为1:3,其中Na2O2既是氧化剂,又是还原剂,已知产物中,除Na2FeO4外,还有Na2O、Na2SO4等,试写出该反应的化学方程式.分析 FeSO4和Na2O2反应,FeSO4与Na2O2的物质的量之比为1:3,已知产物中,除Na2FeO4外,还有Na2O、Na2SO4等,反应中其中Na2O2既是氧化剂,又是还原剂,说明过氧化钠中O元素的化合价即升高又降低,升高时生成氧气,即产物中还有氧气生成,结合原子守恒和电子守恒书写配平方程式.
解答 解:FeSO4和Na2O2反应,FeSO4与Na2O2的物质的量之比为1:3,已知产物中,除Na2FeO4外,还有Na2O、Na2SO4等,反应中其中Na2O2既是氧化剂,又是还原剂,说明过氧化钠中O元素的化合价即升高又降低,升高时生成氧气,即产物中还有氧气生成,所以该反应的反应物为FeSO4和Na2O2,生成物为Na2FeO4、Na2O、2Na2SO4和O2,其反应方程式为2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑;
答:该反应的化学方程式为2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑.
点评 本题考查了氧化还原反应、方程式的书写,题目难度不大,注意把握题中所给的信息,判断出反应物中含有氧气为解题的关键.

练习册系列答案
相关题目
7.在实验室中,对下列实验事故或药品的处理正确的是( )
| A. | 金属钠着火燃烧时,用干燥沙土灭火 | |
| B. | 点燃可燃性气体前,都必须先检验气体的纯度 | |
| C. | 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液擦洗 | |
| D. | 配制H2SO4溶液时,先在量筒中加一定体积的水,再在搅拌下慢慢加入浓H2SO4 |
4.下列反应属于氧化还原反应,但H2O既不做氧化剂,也不做还原剂的是( )
| A. | Cl2+H2O═HCl+HClO | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | 2F2+2H2O═4HF+O2↑ | D. | CaO+H2O═Ca(OH)2 |
11.下列说法正确的是( )
| A. | △H<0、△S>0的反应在温度低时不能自发进行 | |
| B. | 在其他外界条件不变的情况下,使用催化剂可改变化学反应进行的方向 | |
| C. | 因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 | |
| D. | NH4HCO3(s)═NH3 (g)+H2O(g)+CO2 (g)△H=+185.57 kJ/mol可能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
1.向CuSO4溶液中加入铁粉,发生反应得溶液甲;向Fe2(SO4)3溶液中加入铁粉,发生反应[Fe2(SO4)3+Fe═3FeSO4]得溶液乙,下列叙述一定正确的是( )
| A. | 甲与乙所含离子种数完全相同 | B. | 甲与乙所含离子种类完全不同 | ||
| C. | 甲与乙可能含有2种相同的离子 | D. | 甲与乙的颜色一定相同 |
8.下列物质的转变,不能一步实现的( )
| A. | Al2O3→Al(OH)3 | B. | KNO3→KOH | C. | Zn→ZnCl2 | D. | MgCl2→Mg(OH)2 |
16.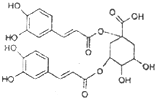 洋蓟属高档蔬菜,从洋蓟提取的物质A具有良好的保健功能和药用价值,A的结构如图.下列关于A的相关叙述正确的是( )
洋蓟属高档蔬菜,从洋蓟提取的物质A具有良好的保健功能和药用价值,A的结构如图.下列关于A的相关叙述正确的是( )
 洋蓟属高档蔬菜,从洋蓟提取的物质A具有良好的保健功能和药用价值,A的结构如图.下列关于A的相关叙述正确的是( )
洋蓟属高档蔬菜,从洋蓟提取的物质A具有良好的保健功能和药用价值,A的结构如图.下列关于A的相关叙述正确的是( )| A. | A在酸性条件下可以发生水解反应 | |
| B. | 1mol A和足量NaOH溶液反应,最多消耗9molNaOH | |
| C. | A能和浓溴水发生加成和取代反应 | |
| D. | 不能与新制得Cu(OH)2反应但能与FeCl3发生显色反应 |
