题目内容
下列化学用语中,不正确的是( )
A、HCl分子的电子式: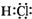 |
B、H2O分子的比例模型: |
C、Mg2+的轨道表示式: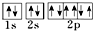 |
D、甲烷分子的球棍模型: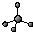 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氯化氢为共价化合物,分子中存在1对Cl-H共用电子对;
B.水分子为V型结构,氧原子体积大于氢原子的体积;
C.2p轨道中电子的自旋方向相同,不满泡利原理;
D.甲烷分子为正四面体结构,分子中存在4个碳氢键.
B.水分子为V型结构,氧原子体积大于氢原子的体积;
C.2p轨道中电子的自旋方向相同,不满泡利原理;
D.甲烷分子为正四面体结构,分子中存在4个碳氢键.
解答:
解:A.氯化氢中存在1个氢氯共价键,氯原子最外层达到8电子稳定结构,氯化氢的电子式为: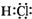 ,故A正确;
,故A正确;
B.水分子的构型为V型,分子中存在两个氧氢键,氧原子半径大于氢离子,水的比例模型为: ,故B正确;
,故B正确;
C.Mg2+的结构中能量最高电子层为L层,含有的2S轨道、2P轨道均全部排满,镁离子正确的轨道表示式为: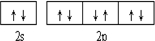 ,故C错误;
,故C错误;
D.甲烷分子中存在4个碳氢共价键,为正四面体结构,甲烷分子的球棍模型为: ,故D正确;
,故D正确;
故选C.
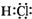 ,故A正确;
,故A正确;B.水分子的构型为V型,分子中存在两个氧氢键,氧原子半径大于氢离子,水的比例模型为:
 ,故B正确;
,故B正确;C.Mg2+的结构中能量最高电子层为L层,含有的2S轨道、2P轨道均全部排满,镁离子正确的轨道表示式为:
 ,故C错误;
,故C错误;D.甲烷分子中存在4个碳氢共价键,为正四面体结构,甲烷分子的球棍模型为:
 ,故D正确;
,故D正确;故选C.
点评:本题考查了电子式、比例模型与球棍模型、轨道表示式的判断,题目难度中等,注意掌握常见的化学用语的概念及表示方法,明确球棍模型与比例模型的区别.

练习册系列答案
相关题目
某元素的气态氢化物符合通式RH3,且氢的质量分数为17.65%,则R的最高价氧化物的化学式是( )
| A、N2O5 |
| B、P2O5 |
| C、CO2 |
| D、SO3 |
下列物质中,S元素的化合价为+6的是( )
| A、S |
| B、H2SO4 |
| C、SO2 |
| D、H2S |
下列说法中正确的是( )
| A、碘和四氯化碳可以用分液漏斗进行分离 |
| B、将O2和H2的混合气体通过灼热的氧化铜,可以除去其中的氢气 |
| C、熔融烧碱时,可以使用铁坩埚 |
| D、加热铝箔,待铝熔化后,可以看到液态铝滴落下来 |
NA代表阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、1mol乙烷(CH3CH3)中含有共价键的数目为6NA |
| B、由CO2和O2组成的混合气体共有NA个分子,其中氧原子数为2NA |
| C、标准状况下,22.4L H2O中含氢原子数为2NA |
| D、制取84消毒液(NaClO),消耗0.5mol氯气转移电子数为NA |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、无色透明的溶液:Na+、Al3+、Cl-、OH- |
| B、pH=1的溶液:Na+、NH4+、Cu2+、NO3- |
| C、与铝反应产生大量氢气的溶液:Na+、K+、Cl-、Al3+ |
| D、使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
下列各组分子中,都属于含有极性键的非极性分子的一组是( )
| A、CO2、H2O |
| B、C2H4、CH4 |
| C、Cl2、C2H2 |
| D、NH3、HCl |
下列物质中,既含离子键又含共价键的是( )
| A、HCl |
| B、NaOH |
| C、NaCl |
| D、O2 |
解决“白色污染”问题,下列做法不宜提倡的是( )
| A、使用新型可降解塑料 |
| B、用布袋代替塑料袋 |
| C、回收废弃塑料 |
| D、焚烧废弃塑料 |