题目内容
NA代表阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、1mol乙烷(CH3CH3)中含有共价键的数目为6NA |
| B、由CO2和O2组成的混合气体共有NA个分子,其中氧原子数为2NA |
| C、标准状况下,22.4L H2O中含氢原子数为2NA |
| D、制取84消毒液(NaClO),消耗0.5mol氯气转移电子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.乙烷中含有6个C-H键和1个C-C键;
B.1个CO2和1个O2分子内都含有2个氧原子;
C.气体摩尔体积只适用于气体;
D.依据反应:Cl2+2NaOH═NaCl+NaClO+H2O分析解答.
B.1个CO2和1个O2分子内都含有2个氧原子;
C.气体摩尔体积只适用于气体;
D.依据反应:Cl2+2NaOH═NaCl+NaClO+H2O分析解答.
解答:
解:A.乙烷中含有6个C-H键和1个C-C键,所以1mol乙烷含有共价键的数目为7NA,故A错误;
B.1个CO2和1个O2分子内都含有2个氧原子,所以由CO2和O2组成的混合气体共有NA个分子,其中氧原子数为2NA,故B正确;
C.水在标准状况下为液体,不能应用气体摩尔体积,故C错误;
D.Cl2+2NaOH═NaCl+NaClO+H2O,反应中氯气既做还原剂又做氧化剂,消耗1mol氯气,转移1mol电子,所以消耗0.5mol氯气转移电子数为0.5NA,故D错误;
故选:B.
B.1个CO2和1个O2分子内都含有2个氧原子,所以由CO2和O2组成的混合气体共有NA个分子,其中氧原子数为2NA,故B正确;
C.水在标准状况下为液体,不能应用气体摩尔体积,故C错误;
D.Cl2+2NaOH═NaCl+NaClO+H2O,反应中氯气既做还原剂又做氧化剂,消耗1mol氯气,转移1mol电子,所以消耗0.5mol氯气转移电子数为0.5NA,故D错误;
故选:B.
点评:本题考查了阿伏伽德罗的应用,题目难度不大,注意气体摩尔体积只适用于气体.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
下列物质能用铁制器皿盛放的是( )
| A、浓硫酸 | B、稀硫酸 |
| C、氯化铜溶液 | D、氯化铁溶液 |
如图所示是五种短周期元素化合价与原子序数的关系,有关说法不正确的是( )
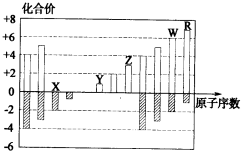

| A、原子半径:R>W>Z>Y>X |
| B、五种原子的核外最外层电子数总和为23 |
| C、X与Y可形成既含离子键又含共价键的化合物 |
| D、X、Y、W可能形成水溶液呈碱性的化合物 |
在25℃的条件下,下列各组离子一定能在指定环境中大量共存的是( )
| A、在c(H+)=10-10mol/L的溶液中:Al3+、NH4+、Cl-、NO3- |
| B、pH=13的溶液中:K+、Na+、SO32-、Cl- |
| C、pH=2的溶液中:K+、NH4+、Cl-、ClO- |
| D、甲基橙呈红色的溶液中:Fe3+、Na+、SO42-、CO32- |
下列烷烃在光照下与氯气反应,只能生成一种一氯代烃的是( )
| A、CH3CH3 |
| B、CH3CH2CH3 |
| C、CH3CH2CH2CH3 |
| D、CH3CH2 CH2CH2CH3 |
下列化学用语中,不正确的是( )
A、HCl分子的电子式: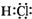 |
B、H2O分子的比例模型: |
C、Mg2+的轨道表示式: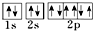 |
D、甲烷分子的球棍模型: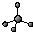 |
标准状况下,448mL HCl气体溶解在少量水里形成1.00mL的溶液,该溶液中HCl的物质的量浓度为( )
| A、5mol?L-1 |
| B、50mol?L-1 |
| C、20.0mol?L-1 |
| D、2.00mol?L-1 |
下列过程或应用不涉及氧化还原反应的是( )
| A、工业上以Cl2和Ca(OH)2为原料制备漂白粉 |
| B、FeCl3溶液“腐蚀”Cu板 |
| C、Na2O2用作呼吸面具的供氧剂 |
| D、利用Al2(SO4)3和氨水反应来制取氢氧化铝 |