题目内容
某元素的气态氢化物符合通式RH3,且氢的质量分数为17.65%,则R的最高价氧化物的化学式是( )
| A、N2O5 |
| B、P2O5 |
| C、CO2 |
| D、SO3 |
考点:原子结构与元素的性质
专题:元素周期律与元素周期表专题
分析:某元素的气态氢化物符合通式RH3,则R元素化合价为-3价,同一元素最高正价与其最低负价的绝对值为8,则R元素最高正价为+5价,RH3中氢的质量分数为17.65%,则R的相对原子质量=
-3=14,则R为N元素,根据化合物中化合价的代数和为0确定其最高价氧化物的化学式.
| 1×3 |
| 17.65% |
解答:
解:某元素的气态氢化物符合通式RH3,则R元素化合价为-3价,同一元素最高正价与其最低负价的绝对值为8,则R元素最高正价为+5价,RH3中氢的质量分数为17.65%,则R的相对原子质量=
-3=14,则R为N元素,在氧化物中O元素显-2价,化合物中各元素化合价的代数和为0,所以其最高价氧化物的化学式为N2O5,
故选A.
| 1×3 |
| 17.65% |
故选A.
点评:本题考查了化学式的确定,明确其最高价与最低价的关系是解本题关键,再结合化合物中各元素化合价的代数和确定其最高价氧化物中N原子和O原子个数比,题目难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
在实验室用盛有5mL饱和Na2CO3 溶液的试管收集1mL 乙酸乙酯后,沿器壁加入0.5mL紫色石蕊试液(整个过程不振荡试管).对可能出现的现象,下列叙述正确的是( )
| A、液体分两层,石蕊层仍呈紫色,有机层呈无色 |
| B、石蕊层为三层,由上而下呈蓝、紫、红色 |
| C、石蕊层有两层,上层呈紫色,下层呈蓝色 |
| D、石蕊层为三层,由上而下呈红、紫、蓝色 |
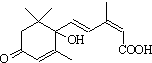 对盆栽鲜花施用了S-诱抗素制剂可保证鲜花盛开.S-诱抗素的分子结构如图,下列关于该物质的说法正确的是( )
对盆栽鲜花施用了S-诱抗素制剂可保证鲜花盛开.S-诱抗素的分子结构如图,下列关于该物质的说法正确的是( )| A、其分子式为C15H22O4 |
| B、1mol该物质与NaOH溶液反应,最多消耗2mol NaOH |
| C、既能发生加聚反应,又能发生缩聚反应 |
| D、既可以与FeCl3溶液发生显色反应,又可以使酸性KMnO4溶液褪色 |
下列物质能用铁制器皿盛放的是( )
| A、浓硫酸 | B、稀硫酸 |
| C、氯化铜溶液 | D、氯化铁溶液 |
 某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据图可得出的判断结论正确的是( )
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据图可得出的判断结论正确的是( )| A、正反应一定是放热反应 |
| B、达到平衡时A2的转化率大小为:b>a>c |
| C、若T2>T1,则正反应一定是吸热反应 |
| D、b点时,平衡体系中A、B原子数之比接近3:1 |
下列各组离子在溶液中因发生氧化还原反应而不能大量共存的是( )
| A、NH4+、K+、Cl-、OH- |
| B、H+、Fe2+、MnO4-、Cl- |
| C、Ba2+、Na+、NO3-、SO42- |
| D、Na+、H+、CO32-、SO42- |
下列各组物质中,不能用酸性高锰酸钾溶液鉴别的是( )
| A、乙酸和乙醛 |
| B、丁二烯和乙烯 |
| C、苯和甲苯 |
| D、丙烯和丙烷 |
下列化学用语中,不正确的是( )
A、HCl分子的电子式: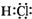 |
B、H2O分子的比例模型: |
C、Mg2+的轨道表示式: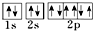 |
D、甲烷分子的球棍模型: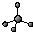 |
 请按要求回答下列问题:
请按要求回答下列问题: