题目内容
下列物质中,既含离子键又含共价键的是( )
| A、HCl |
| B、NaOH |
| C、NaCl |
| D、O2 |
考点:离子化合物的结构特征与性质,共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,第IA族、第IIA族和第VIA族、第VIIA族元素之间易形成离子键,但H元素除外.
解答:
解:A.HCl分子中H原子和Cl原子之间只存在共价键,故A错误;
B.NaOH中钠离子和氢氧根离子之间存在离子键、O原子和H原子之间存在共价键,故B正确;
C.NaCl中钠离子和氯离子之间只存在离子键,故C错误;
D.氧气分子中两个O原子之间只存在共价键,故D错误;
故选B.
B.NaOH中钠离子和氢氧根离子之间存在离子键、O原子和H原子之间存在共价键,故B正确;
C.NaCl中钠离子和氯离子之间只存在离子键,故C错误;
D.氧气分子中两个O原子之间只存在共价键,故D错误;
故选B.
点评:本题考查了离子键和共价键的判断,根据物质的构成微粒确定化学键,不能根据是否含有金属元素判断离子键,为易错点.

练习册系列答案
相关题目
下列各组物质中,不能用酸性高锰酸钾溶液鉴别的是( )
| A、乙酸和乙醛 |
| B、丁二烯和乙烯 |
| C、苯和甲苯 |
| D、丙烯和丙烷 |
下列化学用语中,不正确的是( )
A、HCl分子的电子式: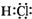 |
B、H2O分子的比例模型: |
C、Mg2+的轨道表示式: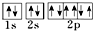 |
D、甲烷分子的球棍模型: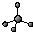 |
常温下,将乙酸和氢氧化钠溶液混合,所得溶液pH=7,则此溶液中( )
| A、c(CH3COO-)>c(Na+) |
| B、c(CH3COO-)<c(Na+) |
| C、c(CH3COO-)=c(Na+) |
| D、无法确定c(CH3COO-)与c(Na+)的关系 |
下列过程或应用不涉及氧化还原反应的是( )
| A、工业上以Cl2和Ca(OH)2为原料制备漂白粉 |
| B、FeCl3溶液“腐蚀”Cu板 |
| C、Na2O2用作呼吸面具的供氧剂 |
| D、利用Al2(SO4)3和氨水反应来制取氢氧化铝 |
根据电子排布的特点,Cu在周期表属于( )
| A、s区 | B、p区 | C、d区 | D、ds区 |
下列有关化学用语表述正确的是( )
A、CO2的电子式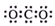 | ||
B、Cl-的结构示意图 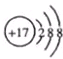 | ||
| C、次氯酸的结构式 H-Cl-O | ||
D、质量数为37的氯原子
|
CO2通入下列各溶液中,不能产生沉淀的是( )
| A、CaCl2溶液 |
| B、Na2SiO3溶液 |
| C、Ca(OH)2溶液 |
| D、Ba(OH)2溶液 |