题目内容
【题目】在实验室以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料制备硼酸(H3BO3),其流程如图1所示,硫酸镁和硼酸的溶解度随温度的变化曲线如图2所示。
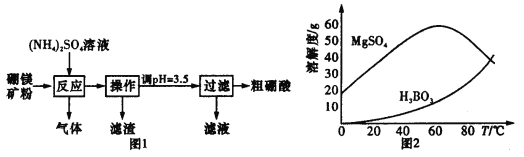
请回答下列问题:
(1)流程中“反应”的实验装置如下图所示:
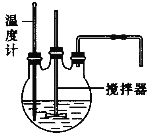
①反应时需控制在95℃进行,控制反应温度的适宜方法是____________________。
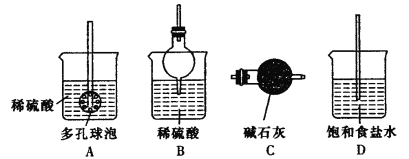
②反应产生的气体需要净化处理,请从下图中选择合适的装置__________(填字母代号)。
(2)实验中得到的粗硼酸还需要重结晶进行提纯,重结晶得到的母液可以在下一次重结晶时重复使用,但达到一定次数后必须净化处理,原因是______________________。
(3)实验时若被强碱溅到,先用大量水冲洗,水洗后再涂上硼酸溶液,写出有关离子方程式:____________。
(4)滴定硼酸时不能直接滴定,因为硼酸是很弱的酸,Ka=5.7×10-10。滴定前,须先将硼酸与甘油作用生成甘油硼酸,Ka=8.4×10-6,然后用酚酞作指示剂,再用NaOH标准溶液滴定。已知硼酸的摩尔质量为61.8 g·mol-1,滴定前称取3.00 g硼酸试样,配成250mL溶液,每次取25.00mL于锥形瓶中滴定,消耗0.200 0 mol·L-1 NaOH标准液的平均体积为20.00 mL。
①计算所得硼酸的纯度=__________。
②若用NaOH标准溶液直接滴定硼酸,则硼酸的纯度将__________(填字母代号)。
A.偏大 B.偏小 C.无影响 D.无法确定
【答案】水浴加热 B 使用一定次数后,母液中杂质的浓度增大,重结晶时会析出杂质影响产品纯度 OH-+H3BO3= H2BO3-+H2O 82.4![]() B
B
【解析】
(1)①水浴加热可以受热均匀,更好的控制温度,所以反应时需控制在95℃进行,控制反应温度的适宜方法是水浴加热;故答案:水浴加热。
②据流程图知硼镁矿粉中加入硫酸铵溶液产生的气体为氨气,氨气极易溶于水,属于碱性气体,所以选择既要防制倒吸,又能和氨气反应的物质进行除杂处理,符合条件的装置为B,故答案:B。
(2)由于使用的次数较多后,母液中杂质的浓度增大,影响产品纯度,所以进行必须净化处理,故答案为:使用一定次数后,母液中杂质的浓度增大,重结晶时会析出杂质影响产品纯度;
(3)硼酸属于一元弱酸,能和强碱反应生成盐和水,所以硼酸和强碱溶液反应有关离子方程式:OH-+H3BO3= H2BO3-+H2O,故答案:OH-+H3BO3= H2BO3-+H2O;
(4) ①设H3BO3浓度为c,若滴定到终点时消耗度为0.200 0 mol·L-1NaOH标准溶液20.00mL,根据 H3BO3~ NaOH关系可知,c(H3BO3)=![]() =0.1600 mol·L-1,所以硼酸的纯度=
=0.1600 mol·L-1,所以硼酸的纯度=![]() =82.4
=82.4![]() ,故答案:82.4
,故答案:82.4![]() ;(
;(
②因为硼酸是很弱的酸,Ka=5.7×10-10,若用NaOH标准溶液直接滴定硼酸,没有突跃,不好观察颜色变化,若用NaOH标准溶液直接滴定硼酸,受水电离的影响,导致硼酸的纯度将偏小,所以答案为B。

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案