��Ŀ����
16��X��Y��Z��W��ԭ������������������ֶ�����Ԫ�أ�X������������Ӧ��ˮ����Ļ�ѧʽΪH2XO3��Y�������������ǵ��Ӳ�����3����Z�ǵؿ��к�����ߵĽ���Ԫ�أ�W��һ�ֺ��ص�������Ϊ28��������Ϊ14������˵����ȷ���ǣ�������| A�� | ԭ�Ӱ뾶�ɴ�С��˳����Z��W��Y��X | |
| B�� | Ԫ�صķǽ�����W��Y��X | |
| C�� | Z2Y3��WX�ֱ������ӻ�������ۻ����� | |
| D�� | X��Z��W����������ﶼ������������ |
���� X��Y��Z��W��ԭ������������������ֶ�����Ԫ�أ�Y�������������ǵ��Ӳ�����3����ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����YΪOԪ�أ�Z�ǵؿ��к�����ߵĽ���Ԫ�أ���ZΪAl��W��һ�ֺ��ص�������Ϊ28��������Ϊ14����ԭ��������=28-14=14����WΪSi��X������������Ӧ��ˮ���ﻯѧʽΪH2XO3������������ϼ�Ϊ+4��ԭ������С��������XΪCԪ�أ��ݴ˽��
��� �⣺X��Y��Z��W��ԭ������������������ֶ�����Ԫ�أ�Y�������������ǵ��Ӳ�����3����ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����YΪOԪ�أ�Z�ǵؿ��к�����ߵĽ���Ԫ�أ���ZΪAl��W��һ�ֺ��ص�������Ϊ28��������Ϊ14����ԭ��������=28-14=14����WΪSi��X������������Ӧ��ˮ���ﻯѧʽΪH2XO3������������ϼ�Ϊ+4��ԭ������С��������XΪCԪ�أ�
A��ͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����ԭ�Ӱ뾶��Z��Al����W��Si����X��C����Y��O������A����
B��ͬ����������ҷǽ�������ǿ��ͬ�������϶��·ǽ����Լ�������Ԫ�صķǽ�����W��Si����X��C����Y��O������B����
C��Al2O3�������ӻ����SiC���ڹ��ۻ������C��ȷ��
D��������̼����������������������������������������������D����
��ѡC��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��ƶ�Ԫ���ǽ���ؼ���ע���Ԫ�������ɵ��������գ�

| A�� | O.1molNa2O2��ˮ��Ӧת�Ƶ�����ĿΪ0.1NA | |
| B�� | ����£�2.24LCl2���µ��ӶԵ���ĿΪ0.2NA | |
| C�� | PH=2��H2SO4��Һ�к�H+����ĿΪ0.12NA | |
| D�� | ��10g��������Ϊ17%�İ�ˮ�У�����H����ĿΪ0.3NA |
| A�� | ���� | B�� | ���� | C�� | Һ�� | D�� | �ѽ� |
| A�� | ת�Ƶĵ�������0.1NA | B�� | ��Ӧ��Һ����������1.6g | ||
| C�� | ���ɵ������к���0.8mol���� | D�� | ��������������1.12L |
| A�� | ���͵����ʶ��Ǹ߷��ӻ����ˮ�������ͬ | |
| B�� | ���ͼ�ϩ����ʹ��ˮ��ɫ��������ˮ�����ӳɷ�Ӧ | |
| C�� | ����̼��������Һ����������Ҵ� | |
| D�� | ����ˮ��ȥ�����л��е������������� |
| A�� | ԭ�Ӱ뾶��W��Z��Y��X | |
| B�� | W���������ڻ�����YW2 | |
| C�� | �⻯����ȶ��Ժͷе����Z��W | |
| D�� | X�����ڼ��ȵ���������Z��ij�ֵ��ʷ�Ӧ����X2Z2 |
| A�� | ʵ���ҵ�Ũ����ͨ���Ի�ɫ | B�� | Fe��NO3��2��Һ�е���ϡ���� | ||
| C�� | NO2������ʪ��ĵ���KI��ֽ���� | D�� | ������̿�����īˮ����ɫ |

 ��C
��C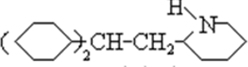 ��
��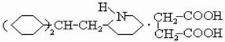 ��
��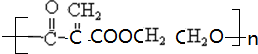 ��
�� ��
��