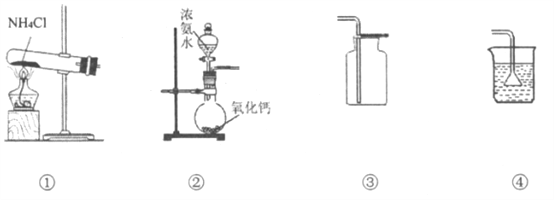
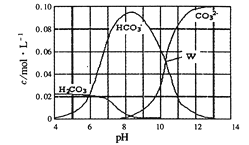
题目内容
【题目】分析下列烃分子,完成填空。
①![]() ②
②  ③
③ 
④ ⑤
⑤ ![]() ⑥
⑥ 
(1)属于烷烃的有___________;互为同系物的有_____、______;(填序号)
(2)任写一种①的同分异构体的结构简式 ___________;
(3)④生成氯乙烷的反应方程式为:________________________;
(4)③在一定条件下与液溴反应方程式为:_______________________;
(5)②与水反应方程式为:________________________;
(6)④的二氯代物有__________种。
【答案】 ①④⑥ ①④⑥ ③⑤ CH3-CH(CH3)-CH2-CH3或(CH3)4C。 ![]()
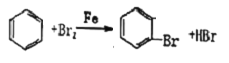 CH=CH2 +H2O
CH=CH2 +H2O![]() CH3CH2OH 2
CH3CH2OH 2
【解析】(1)根据烷烃的通式为CnH2n+2(n≥1)进行判定;同系物指的是组成相同,结构相似,分子间相差nCH2原子团的有机物。
(2)C5H12有3种结构。
(3)乙烷和氯气发生取代反应生成氯乙烷。
(4)苯与液溴在铁作催化剂条件下发生取代反应生成溴苯。
(5)乙烯和水发生加成反应生成乙醇。
(6)乙烷的二氯代物有2种。
(1)六种物质的分子式分别为①为C5H12 ②C2H4③C6H6④C2H6⑤C7H8⑥CH4;烷烃的通式为CnH2n+2 (n≥1), 所以属于烷烃的有:①④⑥;同系物指的是组成相同,结构相似,分子间相差nCH2原子团的有机物,因此互为同系物的有①④⑥和③⑤;正确答案:①④⑥;①④⑥和③⑤。
(2)①为C5H12,其结构除了![]() 外,还有:CH3-CH(CH3)-CH2-CH3 和(CH3)4C;正确答案:CH3-CH(CH3)-CH2-CH3或(CH3)4C。
外,还有:CH3-CH(CH3)-CH2-CH3 和(CH3)4C;正确答案:CH3-CH(CH3)-CH2-CH3或(CH3)4C。
(3)乙烷和氯气光照发生取代反应生成氯乙烷,反应方程式为:![]() ;正确答案:
;正确答案:![]() 。
。
(4)苯和液溴在铁作催化剂条件下发生取代反应生成溴苯和溴化氢,应方程式为 ;正确答案:
;正确答案: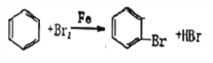 。
。
5)乙烯和水发生加成反应生成乙醇,反应方程式为CH=CH2 +H2O![]() CH3CH2OH;正确答案:CH=CH2 +H2O
CH3CH2OH;正确答案:CH=CH2 +H2O![]() CH3CH2OH。
CH3CH2OH。
(6)两个氯原子连在同一个碳,结构有1种,分别连在两个碳上,结构有1种,共计有2种;乙烷的二氯代物有2种;正确答案:2。

【题目】甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇:
(1)已知:①H2(g)+1/2O2(g)![]() H2O(l) ΔH1=-285.8 kJ/mol;
H2O(l) ΔH1=-285.8 kJ/mol;
②CO (g)+1/2O2 (g)![]() CO2 (g) ΔH2=-283kJ/mol
CO2 (g) ΔH2=-283kJ/mol
③CH3OH(g)+3/2O2(g)![]() CO2(g)+2H2O(l) ΔH3=-764.6 kJ/mol
CO2(g)+2H2O(l) ΔH3=-764.6 kJ/mol
则工业制备甲醇的可逆反应热化学方程式为_______________________________;
(2)恒温恒容条件下,下列描述中能说明上述反应已达平衡状态的是__________。
A.单位时间内生成n mol CO的同时生成2n mol H2 B.ν(H2)正=2ν(CH3OH)逆
C.容器内气体的密度保持不变 D.容器中气体的压强保持不变
(3)某化学研究性学习小组模拟工业合成甲醇的反应,在容积固定为2L的密闭容器内充入1 molCO和 2 molH2,加入合适催化剂(体积可以忽略不计)后在250°C开始反应,CO物质的量随时间变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
n(CO)/mol | 1.00 | 0.79 | 0.63 | 0.54 | 0.50 | 0.50 |
则从反应开始到20min时,以ν(H2)=________,该温度下平衡常数K=_______。
(4)加入催化剂后在250 ℃开始反应,CO的平衡转化率与温度、压强的关系如图所示。
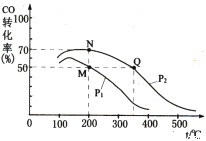
①M、N、Q三点的平衡常数KM、KN、KQ的大小关系为___________________________。
②由M点到N点改变的外界条件是_________。
A、降低温度 B、增大压强
C、改用更好的催化剂 D、通入更多的CO
(5)25℃时以稀硫酸为电解质溶液制成甲醇燃料电池,则负极的电极方程式为_________________________。