题目内容
【题目】甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇:
(1)已知:①H2(g)+1/2O2(g)![]() H2O(l) ΔH1=-285.8 kJ/mol;
H2O(l) ΔH1=-285.8 kJ/mol;
②CO (g)+1/2O2 (g)![]() CO2 (g) ΔH2=-283kJ/mol
CO2 (g) ΔH2=-283kJ/mol
③CH3OH(g)+3/2O2(g)![]() CO2(g)+2H2O(l) ΔH3=-764.6 kJ/mol
CO2(g)+2H2O(l) ΔH3=-764.6 kJ/mol
则工业制备甲醇的可逆反应热化学方程式为_______________________________;
(2)恒温恒容条件下,下列描述中能说明上述反应已达平衡状态的是__________。
A.单位时间内生成n mol CO的同时生成2n mol H2 B.ν(H2)正=2ν(CH3OH)逆
C.容器内气体的密度保持不变 D.容器中气体的压强保持不变
(3)某化学研究性学习小组模拟工业合成甲醇的反应,在容积固定为2L的密闭容器内充入1 molCO和 2 molH2,加入合适催化剂(体积可以忽略不计)后在250°C开始反应,CO物质的量随时间变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
n(CO)/mol | 1.00 | 0.79 | 0.63 | 0.54 | 0.50 | 0.50 |
则从反应开始到20min时,以ν(H2)=________,该温度下平衡常数K=_______。
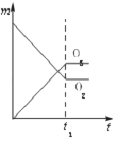
(4)加入催化剂后在250 ℃开始反应,CO的平衡转化率与温度、压强的关系如图所示。
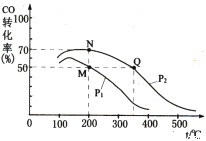
①M、N、Q三点的平衡常数KM、KN、KQ的大小关系为___________________________。
②由M点到N点改变的外界条件是_________。
A、降低温度 B、增大压强
C、改用更好的催化剂 D、通入更多的CO
(5)25℃时以稀硫酸为电解质溶液制成甲醇燃料电池,则负极的电极方程式为_________________________。
【答案】 CO(g)+2H2(g)![]() CH3OH(g)△H=-90 kJ/mol BD 0.025mol/(L·min) 4 (mol/L)-2 KM=KN>KQ B CH3OH-6e-+H2O
CH3OH(g)△H=-90 kJ/mol BD 0.025mol/(L·min) 4 (mol/L)-2 KM=KN>KQ B CH3OH-6e-+H2O![]() CO2↑+6H+
CO2↑+6H+
【解析】(1)反应①×2+反应②-反应③,得到:CO(g)+2H2(g)![]() CH3OH(g)△H=-90 kJ/mol。
CH3OH(g)△H=-90 kJ/mol。
(2)单位时间内生成n mol CO的同时生成2n mol H2,说的都是逆反应,没有说明正反应的情况,所以选项A不能说明反应达平衡。ν(H2)正=2ν(CH3OH)逆,说明了两个方向的速率,且速率比等于系数比,选项B能说明反应达平衡。根据质量守恒定律,总质量不变,总体积也不变,所以密度恒定不变,选项C不能说明反应达平衡。恒容下,容器中气体的压强保持不变,就是气体的物质的量不变,所以选项D能说明反应达平衡。
(3)![]() ,所以
,所以 ![]() = 0.025mol/(L·min)。根据题目数据可计算如下:
= 0.025mol/(L·min)。根据题目数据可计算如下:
CO(g) + 2H2(g)![]() CH3OH(g)
CH3OH(g)
起始: 1 2 0
反应: 0.5 1 0.5
平衡: 0.5 1 0.5
所以CO、H2和CH3OH的平衡浓度分别为:0.25mol/L、0.5mol/L和0.25mol/L,所以反应的平衡常数![]() (mol/L)-2。
(mol/L)-2。
(4)①由图得到M、N、Q三点的温度为:Q>M=N,因为反应放热,K值随温度上升而下降,所以M、N、Q三点的平衡常数KM、KN、KQ的大小关系为:KM=KN>KQ。
②题目中对该图的描述是:CO的平衡转化率与温度、压强的关系如图所示。图中横坐标是温度,表示温度对CO的平衡转化率的影响,所以两条曲线一定代表不同压强,以表示压强对于CO平衡转化率的影响。所以M到N必须变化压强,选项B正确。
(5)甲醇燃料电池的总反应为:CH3OH + 3/2O2 = CO2 + 2H2O,因为电解质为硫酸,所以正极反应为:O2 + 4H+ + 4e- = 2H2O,总反应减去正极反应(注意将正极反应扩大3/2倍),得到负极反应:CH3OH-6e-+H2O![]() CO2↑+6H+。
CO2↑+6H+。

 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案