��Ŀ����
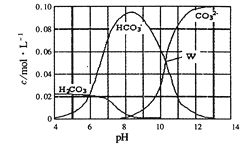
����Ŀ��25��ʱ��0.1 mol Na2CO3�����������õ�һ�����Ϊ1L ����Һ����Һ�в������� pH �Ĺ�ϵ��ͼ��ʾ�������й���Һ������Ũ�ȹ�ϵ������ȷ����
A. W����ʾ����Һ�У�c(Na��)��c(H��)��4c(CO32��)��c(OH��)��c(Cl��)
B. pH��4����Һ�У�c(H2CO3)��c(HCO3��)��c(CO32��)��0.1 mol/L
C. pH=8����Һ�У�c(H��)��2c(H2CO3)��c(HCO3��)��c(OH��)��c(Cl��)
D. pH��11����Һ�У�c(Na��)��c(Cl��)��c(CO32��)��c(HCO3��)��c(H2CO3)
���𰸡�C
��������A�����ݵ���غ��֪����Һ������Ũ��Ӧ�����㣺c(Na+)+c(H+)=2c(CO32-)+c(OH-) +c(Cl-) +c(HCO3-)����A����B������ͼ���֪��pH=4ʱ��CO2���ɣ����������غ��֪c(H2CO3)+c(HCO3-)+c(CO32-)��0.1 molL-1����B����C������ͼ���֪pH=8ʱ����Һ��̼�����Ƶ�Ũ��ԶԶ����̼���Ƶ�Ũ�ȣ���˵����Ӧ��ǡ��������̼�����ƣ�����������غ��֪��c(H2CO3)+c(HCO3-)+c(CO32-)=c(Cl-)=![]() c(Na+)���ٽ�ϵ���غ�c(Na+)+c(H+) =2c(CO32-) +c(OH-)+c(Cl-)+c(HCO3-)�ɵã�c(H+)+2c(H2CO3)+c(HCO3-)=c(OH-)+c(Cl-)����C��ȷ��D������ͼ���֪pH=11ʱ����Һ̼���Ƶ�Ũ��ԶԶ����̼�����ƣ���˵��̼�����ǹ����ģ���c(Na+)��c(CO32-)��c(Cl-)��c(HCO3-)��c(H2CO3)����D����ѡC��
c(Na+)���ٽ�ϵ���غ�c(Na+)+c(H+) =2c(CO32-) +c(OH-)+c(Cl-)+c(HCO3-)�ɵã�c(H+)+2c(H2CO3)+c(HCO3-)=c(OH-)+c(Cl-)����C��ȷ��D������ͼ���֪pH=11ʱ����Һ̼���Ƶ�Ũ��ԶԶ����̼�����ƣ���˵��̼�����ǹ����ģ���c(Na+)��c(CO32-)��c(Cl-)��c(HCO3-)��c(H2CO3)����D����ѡC��

 ��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�
��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�