题目内容
13.根据下列几种粒子的结构示意图,回答问题: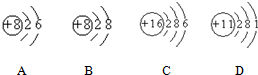
(1)其中属于阴离子的是B(填字母编号),化学式为O2-
(2)属于金属元素的是D(填编号),用${\;}_{Z}^{A}X$来表示该原子的组成${\;}_{11}^{23}Na$.
(3)具有相似化学性质的是AC(填编号).
分析 根据所给的示意图结合质子与电子的关系,可以确定是原子还是离子,阳离子质子数大于电子数,阴离子质子数小于电子数,据此解答即可.
解答 解:(1)B中电子数大于质子数,为带2个负电荷的阴离子,质子数为8,为氧离子,化学式为 O2-,故答案为:B;O2-;
(2)金属元素最外层电子数不超过4个,由所给示意图可以判断D为金属元素Na,Na的相对原子质量为23,那么该元素组成为:${\;}_{11}^{23}Na$,故答案为:D;${\;}_{11}^{23}Na$;
(3)元素的化学性质是由最外层电子数决定的,A和 C的最外层电子数均为6,具有相似的化学性质,故答案为:AC.
点评 本题主要考查的是微粒结构示意图,最外层电子数决定元素的化学性质,本题难度不大,为常考题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列有关高分子化合物的叙述正确的是( )
| A. | 高分子化合物极难溶解 | |
| B. | 高分子化合物依靠分子间作用力结合,材料强度较小 | |
| C. | 高分子均为长链状分子 | |
| D. | 高分子材料均为混合物 |
4.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温下,1L0.1mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| B. | 1mol羟基中电子数为10 NA | |
| C. | 在反应KIO3+6HI═KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6 NA | |
| D. | 常温常压下,22.4L乙烯中C--H键数为4 NA |
8.在标准状况下,2mol氯气的体积是( )
| A. | 100 L | B. | 10 L | C. | 11.2L | D. | 44.8L |
2.下列有关说法正确的是( )
| A. | 一定温度下,反应MgCl2(1)═Mg(1)+Cl2(g)的△H>0,△S>0 | |
| B. | 用pH均为12的NaOH溶液和氨水分别中和等物质的量的HCl,消耗氨水的体积更大 | |
| C. | N2(g)+3H2(g)?2NH3(g) (△H<0),当其他条件不变时,升高温度,H2的反应速率和转化率均增大 | |
| D. | 对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |
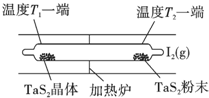 化学反应原理在科研和生产中有广泛应用:
化学反应原理在科研和生产中有广泛应用: