题目内容
2.下列有关说法正确的是( )| A. | 一定温度下,反应MgCl2(1)═Mg(1)+Cl2(g)的△H>0,△S>0 | |
| B. | 用pH均为12的NaOH溶液和氨水分别中和等物质的量的HCl,消耗氨水的体积更大 | |
| C. | N2(g)+3H2(g)?2NH3(g) (△H<0),当其他条件不变时,升高温度,H2的反应速率和转化率均增大 | |
| D. | 对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |
分析 A.MgCl2(1)═Mg(1)+Cl2(g)该反应为吸热、熵值增大的反应;
B.pH=12的NaOH溶液和氨水,氨水的浓度大,所以中和物质的量的HCl,消耗氨水的体积小;
C.升高温度平衡向吸热方向移动;
D.平衡常数只受温度影响.
解答 解:A.MgCl2(1)═Mg(1)+Cl2(g)该反应为吸热、熵值增大的反应,即MgCl2(1)═Mg(1)+Cl2(g)的△H>0,△S>0,故A正确;
B.pH=12的NaOH溶液和氨水,氨水的浓度大,所以中和物质的量的HCl,消耗氨水的体积小,故B错误;
C.N2(g)+3H2(g)?2NH3(g) (△H<0),反应为放热反应,升高温度,平衡向左移动,氢气转化率降低,故C错误;
D.平衡常数只受温度影响,温度不变,平衡常数不变,故D错误;
故选:A.
点评 本题为综合题,考查了焓变与熵变、化学平衡的移动的影响因素、弱电解质的电离,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
12.化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况.下列反应中,属干这种情况的是( )
①过量锌与18 mol/L的硫酸反应;
②过量氢气与少量氮气在催化剂存在下充分反应;
③浓盐酸与过量的MnO2反应;
④过量铜与浓硫酸反应;
⑤过量铜与稀硝酸反应;
⑥过量稀硫酸与大块状石灰石反应.
⑦常温下过量的浓硫酸与铝反应.
①过量锌与18 mol/L的硫酸反应;
②过量氢气与少量氮气在催化剂存在下充分反应;
③浓盐酸与过量的MnO2反应;
④过量铜与浓硫酸反应;
⑤过量铜与稀硝酸反应;
⑥过量稀硫酸与大块状石灰石反应.
⑦常温下过量的浓硫酸与铝反应.
| A. | ②③⑤ | B. | ②③④⑥⑦ | C. | ①④⑤ | D. | ①②③④⑤ |
17.下列事实不能用勒夏特列原理解释的是( )
| A. | 打开啤酒瓶盖,逸出大量气泡 | |
| B. | 实验室可以用排饱和食盐水的方法收集氯气 | |
| C. | 将铜粉和锌粉混合后放入稀硫酸中,产生气体的速率比不加铜粉时的快 | |
| D. | 在pH等于3的醋酸溶液中加入少量CH3COONH4固体,溶液pH增大 |
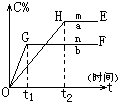 对于反应xA(g)+yB(g)?pC(g)+qD(g).压强与温度对C的质量分数的影响如图所示:
对于反应xA(g)+yB(g)?pC(g)+qD(g).压强与温度对C的质量分数的影响如图所示: