题目内容
【题目】“坚持全民共治、源头防治,持续实施大气污染防治行动,打赢蓝天保卫战!”以NOx为主要成分的雾霾的综合治理是当前重要的研究课题。
(1)工业上采用NH3-SCR法是消除氮氧化物的常用方法。它利用氨在一定条件下将NOx在脱硝装置中转化为N2。主要反应原理为:主反应:
a.4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) ΔH1
4N2(g)+6H2O(g) ΔH1
副反应:b.4NH3(g)+3O2(g) ![]() 2N2(g)+6H2O(g) ΔH2=-1267.1kJ/mol
2N2(g)+6H2O(g) ΔH2=-1267.1kJ/mol
c.4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) ΔH3=-907.3kJ/mol
4NO(g)+6H2O(g) ΔH3=-907.3kJ/mol
①上述反应中利用了NH3的__________性质;ΔH1=____________。
②将氮氧化合物按一定的流速通过脱硝装置,测得出口的NO残留浓度与温度的关系如图1,试分析脱硝的适宜温度是______(填序号)。
A.<850℃ b.900~1000℃ c.>1050℃
温度超过1000℃,NO浓度升高的原因是_____________________________________。
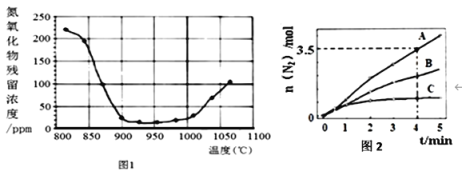
(2)已知:8NH3(g)+6NO2(g)![]() 7N2(g) +12H2O(l) ΔH<0。相同条件下,在2 L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间变化如图2所示。下列说法正确的是_______(填标号)。
7N2(g) +12H2O(l) ΔH<0。相同条件下,在2 L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间变化如图2所示。下列说法正确的是_______(填标号)。
a.使用催化剂A达平衡时,ΔH值更大
b.升高温度可使容器内气体颜色加深
c.单位时间内形成N-H键与O-H键的数目相等时,说明反应已经达到平衡
d.若在恒容绝热的密闭容器中反应,当平衡常数不变时,说明反应已经达到平衡
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-746.8k·mol-1,实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,v正___v逆(填“>”“<”或“=”)。
②若在1L的密闭容器中充入1mol CO和1mol NO,在一定温度下达到平衡时,CO的转化率为40%,则![]() =___________。(分数表示)。
=___________。(分数表示)。
【答案】还原性 -1626.9 kJ/mol b 高温下,副反应c,产生了NO;主反应a正反应为放热反应,升高温度,平衡逆向移动,也会导致NO的浓度增大 b c d < ![]()
【解析】
(1)①分析反应原理,在反应中NH3中N原子化合价升高,发生氧化反应,说明NH3具有还原性,利用了NH3的还原性;分析a、b、c反应,可知反应a=2b-c,则ΔH1=![]() ;答案为:还原性;-1626.9 kJ/mol;
;答案为:还原性;-1626.9 kJ/mol;
②分析图1中NO残留浓度与温度的关系,可知,在900~1000℃时,NO残留浓度最低,故脱硝的适宜温度为900~1000℃;分析反应原理,高温下,副反应c也会产生NO。主反应a的正反应为放热反应,升高温度,平衡逆向移动,导致NO浓度增大;答案为:b;高温下,副反应c,产生了NO;主反应a正反应为放热反应,升高温度,平衡逆向移动,也会导致NO的浓度增大
(2)a.催化剂不影响平衡移动,所以反应的焓变不变,a项错误;
b.该反应的正反应为放热反应,升高温度平衡逆向移动,二氧化氮的浓度增大,气体颜色加深,b项正确;
c.单位时间内形成N-H键与O-H键的数目相等时,正逆反应速率相等,反应达到平衡状态,c项正确;
d.若在恒容绝热的密闭容器中反应,随着反应进行,化学平衡常数改变,当化学平衡常数不变时,正逆反应速率相等,反应达到平衡状态,d项正确;
答案选bcd;答案为:bcd;
(3)①该反应为放热反应,升高温度,平衡逆向移动,此时v正<v逆;答案为:<;
②若在1L的密闭容器中充入1mol CO和1mol NO,在一定温度下达到平衡时,CO的转化率为40%,根据题意有:
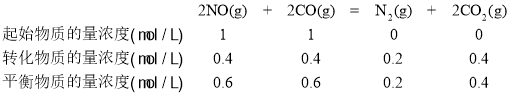
反应达平衡时,v正<v逆,即k正·c2(NO)·c2(CO)=k逆·c(N2)·c2(CO2),则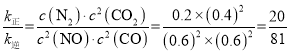 ,答案为:
,答案为:![]() 。
。

【题目】下列“实验结论”与“实验操作及现象”相符的一组是( )
选项 | 实验操作及现象 | 实验结论 |
A | 向某溶液中加入 | 该溶液中一定含有 |
B | 向某溶液中加入稀盐酸,有无色气体产生 | 该溶液中一定含有 |
C | 向某溶液中加入 | 该溶液中一定含有 |
D | 向某溶液中加入 | 该溶液中一定含有 |
A.AB.BC.CD.D
【题目】下表为元素周期表的一部分,针对表中①~⑧元素,回答下列问题
① | |||||||||||||||
② | ③ | ④ | |||||||||||||
⑤ | ⑥ | ⑦ | ⑧ |
(1)③元素在周期表中的位置是第二周期第_____________族
(2)写出②的最高价氧化物的电子式_____________
(3)⑤和⑥两种元素的最高价氧化物对应水化物中碱性较强的是_____________(填化学式)
(4)写出③和⑦的常见氢化物中稳定性较好的的物质的电子式_____________
(5)写出⑤⑧的最高价氧化物对应水化物互相反应的离子方程式_____________