题目内容
【题目】喷泉是一种常见的现象,其产生的原理是存在压强差(如图所示)。
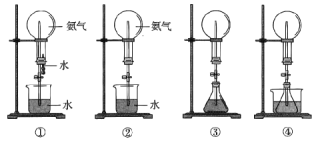
试回答下列问题:
(1)实验室制取氨气的化学方程式为_________________________________。
①用图①装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发喷泉的操作是_____________。
②如果只提供图②的装置,请说明引发喷泉的方法:______________________。
(2)利用图③装置,在锥形瓶中分别加入足量的下列物质,反应后可能产生喷泉的是______。
A.Cu与稀盐酸 B.Fe和稀硫酸 C.Cu与稀硝酸 D.NaHCO3溶液与NaOH溶液
(3)在图④锥形瓶中加入酒精瓶外放一水槽,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉,水槽中加入的物质可能是___________。
A.浓硫酸 B.食盐 C.硝酸钾 D.硫酸铜
(4)同温同压下,两个等体积的干燥圆底烧瓶中分别充满NH3和NO2,进行喷泉实验,如图所示,经充分反应后,发现烧瓶①中充满液体,②中充有![]() 体积的液体,则两烧瓶内溶质的物质的量浓度的正确关系是______
体积的液体,则两烧瓶内溶质的物质的量浓度的正确关系是______
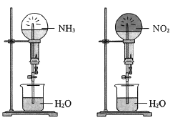
A.①>② B.①<② C.①=② D.不能确定
【答案】2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O 打开止水夹,挤出胶头滴管中的水; 打开止水夹,用热毛巾捂住圆底烧瓶至有气泡从水中冒出,移去热毛巾 BC A C
CaCl2+2NH3↑+2H2O 打开止水夹,挤出胶头滴管中的水; 打开止水夹,用热毛巾捂住圆底烧瓶至有气泡从水中冒出,移去热毛巾 BC A C
【解析】
(1)实验室用氯化铵、氢氧化钙加热制取氨气;利用氨气极易溶于水,形成压强差而形成喷泉;
(2)利用图③装置,若锥形瓶中的物质相互反应生成气体,锥形瓶内压强增大,可形成喷泉;
(3)浓硫酸溶于水放热,使乙醇汽化变为气体,锥形瓶内压强增大,形成喷泉;
(4)根据![]() 计算物质的量浓度。
计算物质的量浓度。
(1)实验室用氯化铵、氢氧化钙加热制取氨气,反应方程式是2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
①用图①装置进行喷泉实验,引发喷泉的操作是:氨气极易溶于水,打开止水夹,挤出胶头滴管中的水,氨气溶于水后烧瓶内压强迅速减小,而形成喷泉;
②如果只提供图②的装置,引发喷泉的方法是:打开止水夹,用热毛巾捂住圆底烧瓶至有气泡从水中冒出,氨气溶于水后烧瓶内压强迅速减小,而形成喷泉;
(2) A.Cu与稀盐酸不反应,不能生成气体,不能形成喷泉,故不选A;
B.Fe和稀硫酸反应生成氢气,锥形瓶内气压强增大,能形成喷泉,故选B;
C.Cu与稀硝酸反应生成NO气体,锥形瓶内气压强增大,能形成喷泉,故选C;
D.NaHCO3溶液与NaOH溶液反应生成碳酸钠和水,瓶内气体不能增多,不能形成喷泉,故不选D;
(3)浓硫酸溶于水放热,使乙醇汽化变为气体,锥形瓶内压强增大,形成喷泉,故选A;
(4)设烧瓶的体积是VL,则n(NH3)=![]() ,所以氨水的浓度是
,所以氨水的浓度是![]() ÷VL=
÷VL=![]() ; n(NO2)=
; n(NO2)=![]() ,根据方程式3NO2+H2O=2HNO3+NO, n(HNO3)=
,根据方程式3NO2+H2O=2HNO3+NO, n(HNO3)= ![]() ,c(HNO3)=
,c(HNO3)= ![]() ÷
÷![]() L=
L=![]() ,两烧瓶内溶质的物质的量浓度的正确关系是①=②,选C。
,两烧瓶内溶质的物质的量浓度的正确关系是①=②,选C。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案