题目内容
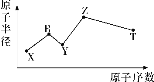
【题目】如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )

A.原子半径:Z>Y>X
B.气态氢化物的热稳定性:W>R
C.WX3和水反应生成的化合物是离子化合物
D.X元素在自然界中存在同素异形现象
【答案】D
【解析】
由图中化合价可知,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+1价,处于IA族,原子序数大于O元素,故Y为Na元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,R的最高正价为+7价,应为Cl元素,所以X为O, Y为Na, Z为Al, W为S,R为Cl。
A.根据分析,X为O,Y为Na, Z为Al,所以原子半径应为Na> Al>O,A错误;
B.根据分析,W为S,R为Cl,由于非金属性Cl>S,则气态氢化物的稳定性HCl>H2S,B错误;
C.根据分析,X为O,W为S,所以SO3和水反应形成的化合物是H2SO4,是共价化合物,C错误;
D.X为O,自然界中有O2和O3两种同素异形体,D正确;
答案选D

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目