题目内容
6.下列推断正确的是( )| A. | 共价键只有方向性 | |
| B. | 离子晶体中只存在阴阳离子间的静电吸引力 | |
| C. | Na2O2中阴阳离子个数比为1:2 | |
| D. | 化学式CO2、SiO2、NaCl、CaH2都可以表示分子 |
分析 A.共价键具有方向性和饱和性;
B.存在阴阳离子间的静电吸引力和排斥力;
C.过氧化钠中过氧根离子显-2价;
D.SiO2、NaCl、CaH2分别为原子晶体、离子晶体,不存在分子.
解答 解:A.共价键具有方向性和饱和性,如氢气分子为H2而不是H3,说明共价键具有饱和性,故A错误;
B.离子键为阴阳离子之间的作用力,包括静电吸引力和排斥力,故B错误;
C.过氧化钠中过氧根离子显-2价,其电子式是 ,晶体中阴阳离子个数比为1:2,故C正确;
,晶体中阴阳离子个数比为1:2,故C正确;
D.SiO2、NaCl、CaH2分别为原子晶体、离子晶体,不存在分子,只有分子晶体存在分子,故D错误.
故选C.
点评 本题考查较为综合,涉及共价键、晶体类型等知识,为高频考点,注意把握晶体类型和共价键的相关知识,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
17.不属于高分子化合物的正确组合是( )
①甘油 ②油脂 ③纤维素 ④淀粉 ⑤有机玻璃 ⑥蛋白质 ⑦蔗糖 ⑧天然橡胶 ⑨2,4,6-三硝基甲苯(TNT) ⑩涤纶.
①甘油 ②油脂 ③纤维素 ④淀粉 ⑤有机玻璃 ⑥蛋白质 ⑦蔗糖 ⑧天然橡胶 ⑨2,4,6-三硝基甲苯(TNT) ⑩涤纶.
| A. | ①④⑥⑦ | B. | ①②⑦⑨ | C. | ③⑤⑥⑩ | D. | ②③⑦⑧ |
14.在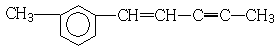 分子中,下列说法正确的是( )
分子中,下列说法正确的是( )
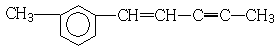 分子中,下列说法正确的是( )
分子中,下列说法正确的是( )| A. | 处于同一平面上的原子数最多可能有12个 | |
| B. | 1mol该分子最多可以与3molH2加成 | |
| C. | 该分子含有三种官能团 | |
| D. | 该物质能使溴水和高锰酸钾溶液褪色 |
11.下列叙述正确的是( )
| A. | 同周期元素的原子半径以ⅦA族的为最大 | |
| B. | 在周期表中0族元素的电负性最大 | |
| C. | ⅠA族元素的原子,其半径越大第一电离能越小 | |
| D. | 所有主族元素的原子形成单原子离子时的最高价数都和它的族数相等 |
15.已知1-18号元素的离子aAm+、bBn+、cCp-、dDq-都具有相同的电子层结构,下列关系正确的是( )
| A. | 若p>q,则还原性cCp-<dDq- | |
| B. | 若m>n,则碱性A(OH)m>B(OH)n | |
| C. | 若半径aAm+>bBn+,则a<b | |
| D. | 若半径aAm+>bBn+,则A的单质一定能从含Bn+的盐溶液中置换出B |
16.下列说法中正确的是( )
| A. | H2O2的电子式: | |
| B. | ${\;}_{17}^{35}$Cl- 与${\;}_{17}^{37}$Cl属同位素 | |
| C. | 单质气体分子中不一定都具有共价键 | |
| D. | CaCl2晶体中既含有离子键又含有共价键 |

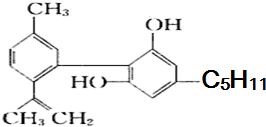 大麻酚及它的衍生物都属麻醉药品,并且毒性较强.吸食大麻使人的脑功能失调、记忆力消退、健忘、注意力很难集中,而且由于大麻中焦油含量高,其致癌率也较高.大麻酚分子结构为:
大麻酚及它的衍生物都属麻醉药品,并且毒性较强.吸食大麻使人的脑功能失调、记忆力消退、健忘、注意力很难集中,而且由于大麻中焦油含量高,其致癌率也较高.大麻酚分子结构为: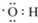 ,它与足量的溴水反应最多消耗Br23mol.
,它与足量的溴水反应最多消耗Br23mol.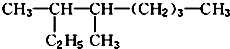 的名称是3,4-二甲基辛烷
的名称是3,4-二甲基辛烷 .
.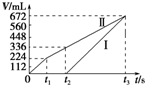 常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图中Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:(要求写出计算步骤)
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图中Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:(要求写出计算步骤)