题目内容
14.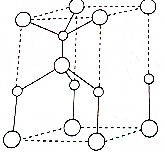 利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,如图为其晶胞结构水土,则每个晶胞中含有B原子的个数为2,该功能陶瓷的化学式为BN.
利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,如图为其晶胞结构水土,则每个晶胞中含有B原子的个数为2,该功能陶瓷的化学式为BN.
分析 同一周期元素中,原子半径随着原子序数增大而减小,根据图中原子半径知,大球是B原子、小球是N原子,B原子个数=1+8×$\frac{1}{8}$=2,N原子个数=1+4×$\frac{1}{4}$=2,根据N、B原子个数比确定化学式.
解答 解:同一周期元素中,原子半径随着原子序数增大而减小,根据图中原子半径知,大球是B原子、小球是N原子,B原子个数=1+8×$\frac{1}{8}$=2,N原子个数=1+4×$\frac{1}{4}$=2,该晶胞中B、N原子个数之比=2:2=1:1,所以化学式为BN,故答案为:2;BN.
点评 本题考查晶胞计算,为高频考点,侧重考查学生分析及空间想象能力,利用均摊法分析计算即可,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列各组顺序的排列正确的是( )
| A. | 金属性:Li<Mg<Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性:H2SO4<H2CO3<HNO3 | D. | 沸点:H2O>H2S>H2Se |
5.将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)?2G(g).忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示.下列说法错误的是( )
体积分数/% 压强/MPa 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1 000 | e | f | 83.0 |
| A. | a<54.0 | B. | b>f | ||
| C. | 915℃,2.0 MPa时E的转化率为60% | D. | K(1000℃)>K(810℃) |
9.下列每组中两种物质反应时,无论哪种过量都可用同一离子方程式表示的是( )
| A. | FeBr2溶液与Cl2 | B. | Ca(HCO3)2溶液与KOH溶液 | ||
| C. | NaHCO3溶液与Al2(SO4)3溶液 | D. | NaHSO4溶液与Ba(OH)2溶液 |
19.向氢氧化钠溶液中通入一定量的二氧化硫气体,再将溶液在减压条件下蒸干,得到一白色固体,此固体的成分不可能是( )
| A. | Na2SO3和NaOH | B. | NaHSO3 | C. | Na2SO3和NaHSO3 | D. | NaHSO3和NaOH |
6.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 32g O2所含的原子数目为NA | |
| B. | 0.5mol H2O所含有的原子数为0.5NA | |
| C. | 1mol H2含有的原子数目为2NA | |
| D. | 0.5NA个氧气分子的物质的量是0.5mol |
3.下列关于SO2和CO2的说法不正确的是( )
| A. | SO2和CO2均是酸酐 | |
| B. | SO2能使品红溶液褪色而CO2则不能 | |
| C. | SO2和CO2均能跟石灰水反应生成白色沉淀 | |
| D. | SO2和CO2均既有氧化性又有还原性 |