题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.用含0.1molFeCl3的饱和溶液制取Fe(OH)3胶体得0.1NA个胶粒
B.将含有NA个Al3+的AlCl3溶液完全蒸干,可得到1mol的固体AlCl3
C.电解法精炼铜,当电路中有0.2NA个电子转移时,阳极的质量一定减轻6.4g
D.25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目约为0.1NA
【答案】D
【解析】
A.Fe(OH)3胶体粒子是氢氧化铁的集合体,制得的胶体中含Fe(OH)3胶体胶粒数目小于0.1NA个,A项错误;
B.AlCl3溶液加热时水解生成Al(OH)3,生成的HCl易挥发,故AlCl3溶液蒸干最终生成Al(OH)3,不能得到固体AlCl3,B项错误;
C.电解精炼铜时,阳极上放电的不止是铜,还有比铜活泼的金属,当电路中有0.2NA个电子转移时,阳极的质量不是减轻6.4g,C项错误;
D.25℃时,pH=13的Ba(OH)2溶液中![]() ,
,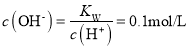 ,则1.0LBa(OH)2溶液中含有的OH-数目约为0.1NA,D项正确;
,则1.0LBa(OH)2溶液中含有的OH-数目约为0.1NA,D项正确;
答案选D。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】某学习小组用下列装置完成了探究浓硫酸和 SO2性质的实验(部分夹持装置已省略),下列“ 现象预测” 与“ 解释或结论” 均正确的是
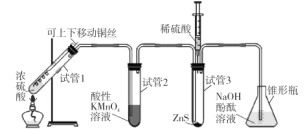
选项 | 仪器 | 现象预测 | 解释或结论 |
A | 试管1 | 有气泡、酸雾,溶液中有白色固体出现 | 酸雾是SO2所形成,白色固体是硫酸铜晶体 |
B | 试管2 | 紫红色溶液由深变浅,直至褪色 | SO2具有还原性 |
C | 试管3 | 注入稀硫酸后,没有现象 | 由于Ksp(ZnS)太小,SO2与ZnS在注入稀硫酸后仍不反应 |
D | 锥形瓶 | 溶液红色变浅 | NaOH溶液完全转化为NaHSO3溶液,NaHSO3溶液碱性小于NaOH |
A.AB.BC.CD.D