题目内容
人工固氮是指将氮元素由游离态转化为化合态的过程.据报道,常温、常压、光照条件下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成的主要产物为NH3,相应的热化学方程式为:
N2(g)+3H2O(l)?2NH3(g)+
O2(g)△H=+765.0kJ/mol.
目前工业合成氨的原理是:N2(g)+3H2(g)?2NH3(g)△H=-93.0kJ/mol.
回答下列问题:
(1)表示氢气燃烧热的热化学方程式为 .
(2)在恒温恒容密闭容器中进行N2和H2合成氨反应,下列能表示达到平衡状态的是 .
a.混合气体的压强不再发生变化
b.混合气体的密度不再发生变化
c.反应容器中N2、NH3的物质的量的比值不再发生变化
d.单位时间内断开a个NN键的同时形成6a个N-H键
e.三种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比
(3)在恒温恒容的密闭容器中,合成氨反应的各物质浓度变化曲线如图所示.请回答下列问题:
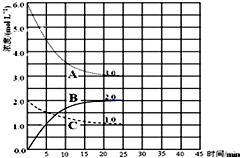
①前25min内,用H2的浓度变化表示的化学反应平均速率是 .
②在25min末反应刚好达到平衡,则该温度下反应的平衡常数K= (计算结果可用分数表示).若升高温度,该反应的平衡常数值将 (填“增大”、“减小”或“不变”).
(4)在一定温度下,将1mol N2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol.
①达平衡时,H2的转化率α1= .
②在相同条件下,若起始时只将NH3置于该容器中,达到平衡状态时NH3的转化率为α2,当α1+α2=1时,则起始时n(NH3)= mol.
N2(g)+3H2O(l)?2NH3(g)+
| 3 |
| 2 |
目前工业合成氨的原理是:N2(g)+3H2(g)?2NH3(g)△H=-93.0kJ/mol.
回答下列问题:
(1)表示氢气燃烧热的热化学方程式为
(2)在恒温恒容密闭容器中进行N2和H2合成氨反应,下列能表示达到平衡状态的是
a.混合气体的压强不再发生变化
b.混合气体的密度不再发生变化
c.反应容器中N2、NH3的物质的量的比值不再发生变化
d.单位时间内断开a个NN键的同时形成6a个N-H键
e.三种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比
(3)在恒温恒容的密闭容器中,合成氨反应的各物质浓度变化曲线如图所示.请回答下列问题:

①前25min内,用H2的浓度变化表示的化学反应平均速率是
②在25min末反应刚好达到平衡,则该温度下反应的平衡常数K=
(4)在一定温度下,将1mol N2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol.
①达平衡时,H2的转化率α1=
②在相同条件下,若起始时只将NH3置于该容器中,达到平衡状态时NH3的转化率为α2,当α1+α2=1时,则起始时n(NH3)=
考点:物质的量或浓度随时间的变化曲线,反应热和焓变,化学平衡的影响因素
专题:化学平衡专题
分析:(1)已知①2N2(g)+6H2O(l)?4NH3(g)+3O2(g)△H=+1530.0kJ/mol.
②N2(g)+3H2(g)?2NH3(g)△H=-93.0kJ/mol,利用盖斯定律将
可得氢气燃烧的热化学方程式;
(2)达到平衡时,正逆反应速率相等,各物质的浓度不变,以此衍生的一些物理量也不变,以此判断是否达到平衡状态;
(3)①根据图象中的浓度变化及时间计算出用H2的浓度变化表示的化学反应平均速率;
②根据平衡常数表达式计算出该反应的平衡常数;升高温度,平衡逆向移动,该反应的平衡常数值将减小;
(4)①设平衡时有x molN2转化,计算出转化的氮气的物质的量,再计算出氮气的转化率;
②α1 +α2 =1,说明这两个反应达到平衡时的状态完全相同,即加入的氨气为2mol.
②N2(g)+3H2(g)?2NH3(g)△H=-93.0kJ/mol,利用盖斯定律将
| ②×2-① |
| 6 |
(2)达到平衡时,正逆反应速率相等,各物质的浓度不变,以此衍生的一些物理量也不变,以此判断是否达到平衡状态;
(3)①根据图象中的浓度变化及时间计算出用H2的浓度变化表示的化学反应平均速率;
②根据平衡常数表达式计算出该反应的平衡常数;升高温度,平衡逆向移动,该反应的平衡常数值将减小;
(4)①设平衡时有x molN2转化,计算出转化的氮气的物质的量,再计算出氮气的转化率;
②α1 +α2 =1,说明这两个反应达到平衡时的状态完全相同,即加入的氨气为2mol.
解答:
解:(1)已知①2N2(g)+6H2O(l)?4NH3(g)+3O2(g)△H=+1530.0kJ/mol.
②N2(g)+3H2(g)?2NH3(g)△H=-93.0kJ/mol,利用盖斯定律将
可得H2(g)+
O2(g)=H2O(l)△H=-286.0 kJ/mol,
故答案为:H2(g)+
O2(g)=H2O(l)△H=-286.0 kJ/mol;
(2)a.混合气体的压强不再发生变化,在恒温恒容密闭容器中,因为合成氨是气体分子数目减小的反应,混合气体的压强不再发生变化,说明达到平衡状态,故a正确;
b.混合气体的密度一直不发生变化,故b错误;
c.反应容器中N2、NH3的物质的量的比值不再发生变化,说能达到平衡,故c正确;
d.无论是否达到平衡状态,都存在单位时间内断开3a个H-H键的同时形成6a个N-H键,不能说明达到平衡状态,故d错误;
e.三种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比,三种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比可能只是某一时刻的比值,不能证明是否达到平衡,故e错误;.
故答案为:ac;
(3)①根据图象可知曲线A代表氢气,v(H2)=
mol?L-1?min-1=0.12mol?L-1?min-1,故答案为:0.12 mol?L-1?min-1;
③在25 min 末反应刚好达到平衡,K=
=
=
;该反应是放热反应,若升高温度,平衡逆向移动,该反应的平衡常数值将减小,
故答案为:
(或0.148、0.15);减小;
(4)①设平衡时有x molN2转化,
N2(g)+3H2(g)?2NH3(g)
起始物质的量:1mol 3mol 0
变化的物质的量:x 3x 2x
平衡物质的量:1-x 3-3x 2x
列式可得:4-2x=2.8,
解得x=0.6mol,α1 =
×100%=60%,
故答案为:60%;
②由α1 +α2 =1,说明这两个反应达到平衡时的状态完全相同,即加入的氨气为2mol,故答案为:2.
②N2(g)+3H2(g)?2NH3(g)△H=-93.0kJ/mol,利用盖斯定律将
| ②×2-① |
| 6 |
| 1 |
| 2 |
故答案为:H2(g)+
| 1 |
| 2 |
(2)a.混合气体的压强不再发生变化,在恒温恒容密闭容器中,因为合成氨是气体分子数目减小的反应,混合气体的压强不再发生变化,说明达到平衡状态,故a正确;
b.混合气体的密度一直不发生变化,故b错误;
c.反应容器中N2、NH3的物质的量的比值不再发生变化,说能达到平衡,故c正确;
d.无论是否达到平衡状态,都存在单位时间内断开3a个H-H键的同时形成6a个N-H键,不能说明达到平衡状态,故d错误;
e.三种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比,三种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比可能只是某一时刻的比值,不能证明是否达到平衡,故e错误;.
故答案为:ac;
(3)①根据图象可知曲线A代表氢气,v(H2)=
| 6.0-3.0 |
| 25 |
③在25 min 末反应刚好达到平衡,K=
| c(NH3)2 |
| c(N2)?c(H2)3 |
| 4 |
| 1×32 |
| 4 |
| 27 |
故答案为:
| 4 |
| 27 |
(4)①设平衡时有x molN2转化,
N2(g)+3H2(g)?2NH3(g)
起始物质的量:1mol 3mol 0
变化的物质的量:x 3x 2x
平衡物质的量:1-x 3-3x 2x
列式可得:4-2x=2.8,
解得x=0.6mol,α1 =
| 0.6mol |
| 1mol |
故答案为:60%;
②由α1 +α2 =1,说明这两个反应达到平衡时的状态完全相同,即加入的氨气为2mol,故答案为:2.
点评:本题考查较综合,涉及知识点较多,注意通过图象分析化学反应速率、化学平衡及计算问题,需要学生较强的观察能力及思维能力,难度较大.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
下列物质中,既含离子键又含共价键的是( )
| A、HCl |
| B、NaOH |
| C、NaCl |
| D、O2 |
解决“白色污染”问题,下列做法不宜提倡的是( )
| A、使用新型可降解塑料 |
| B、用布袋代替塑料袋 |
| C、回收废弃塑料 |
| D、焚烧废弃塑料 |
 右图是某型号进口电池外壳上的标志及说明文字,请认真阅读并按要求回答问题:
右图是某型号进口电池外壳上的标志及说明文字,请认真阅读并按要求回答问题: