题目内容
【题目】用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2 g含有少量中性易溶杂质的样品,配成500 mL待测溶液。称量时,样品可放在________(填字母)称量。
A.小烧杯中 B.洁净纸片上 C.托盘上
(2)滴定过程中,眼睛应注视________________。滴定时,用0.2000molL-的盐酸来滴定待测液,不可选用______(填编号字母)作指示剂。
A.甲基橙 B.石蕊 C.酚酞
(3)滴定时,用0.200 0 mol·L-1的盐酸来滴定待测溶液,根据下表数据,计算被测烧碱溶液的物质的量浓度是________ mol·L-1,烧碱样品的纯度是________。
滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
(4)下列实验操作会对滴定结果产生什么后果?(填“偏高”、“偏低”或“无影响”)
①若将锥形瓶用待测液润洗,然后加入10.00mL待测液,则滴定结果______
②若锥形瓶未干燥就加入10.00mL待测液,则滴定结果______。
【答案】A 锥形瓶内溶液颜色的变化 B 0.4000 97.56% 偏高 无影响
【解析】
(1)易潮解的药品,必须放在玻璃器皿上(如小烧杯、表面皿)里称量;
(2)酸碱中和滴定时,可用酚酞或甲基橙做指示剂,石蕊变色范围宽且现象不明显,故一般不用石蕊作指示剂;
(3)根据c(待测)=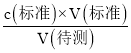 ,V(标准)用两次的平均值;根据m=cVM计算500mL溶液中氢氧化钠的质量,再根据质量分数公式计算氢氧化钠的质量分数;
,V(标准)用两次的平均值;根据m=cVM计算500mL溶液中氢氧化钠的质量,再根据质量分数公式计算氢氧化钠的质量分数;
(4)根据c(待测)=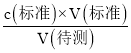 分析不当操作对V(标准)的影响,以此判断浓度的误差。
分析不当操作对V(标准)的影响,以此判断浓度的误差。
(1)烧碱易潮解,必须放在玻璃器皿上(如小烧杯、表面皿)里称量,故答案为A;
(2)滴定过程中,眼睛应注视锥形瓶内溶液颜色的变化;酸碱中和滴定时,可用酚酞或甲基橙做指示剂,石蕊变色范围宽且现象不明显,故一般不用石蕊作指示剂,故答案为B;
(3)第一次消耗的标准液的体积为:(20.50-0.40)mL=20.10mL,第二次消耗的标准液体积为:24.00mL-4.10mL=19.90mL,两次滴定数据都是有效的,所以消耗标准液平均体积为20.00mL,根据c(待测)=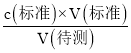 =
=![]() =0.4000molL-1,样品中含有烧碱的质量为:m(烧碱)=cVM=0.4000molL-1×0.5L×40g/mol=8.0g,烧碱的质量分数为:ω=
=0.4000molL-1,样品中含有烧碱的质量为:m(烧碱)=cVM=0.4000molL-1×0.5L×40g/mol=8.0g,烧碱的质量分数为:ω=![]() ×100%=97.56%;
×100%=97.56%;
(4)①若将锥形瓶用待测液润洗,然后加入10.00mL待测液,待测液的物质的量偏大,造成V(标准)偏高,根据c(待测)=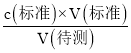 分析,可知c(待测)偏高;
分析,可知c(待测)偏高;
②若锥形瓶未干燥就加入10.00mL待测液,V(标准)无影响,根据c(待测)=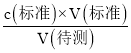 分析,可知c(待测)无影响。
分析,可知c(待测)无影响。