题目内容
18.区别CH4和C2H4的方法最好是( )| A. | 通入溴水中观察溶液颜色的变化 | B. | 嗅闻它们的气味 | ||
| C. | 比较它们在水中的溶解度大小 | D. | 点燃它们后,观察火焰 |
分析 乙烯含有C=C官能团,与溴水发生加成反应而使溴水褪色,能与酸性高锰酸钾溶液发生氧化还原反应而使高锰酸钾溶液褪色,点燃时甲烷和乙烯火焰颜色都呈蓝色,甲烷性质较稳定.
解答 解:A.乙烯含有C=C官能团,与溴水发生加成反应而使溴水褪色,甲烷和溴水不反应,可鉴别,故A正确;
B.都为无色无味气体,不能鉴别,故B错误;
C.都不溶于水,不能鉴别,故C错误;
D.点燃时甲烷和乙烯火焰颜色都呈蓝色,不能鉴别,故D错误.
故选A.
点评 本题考查甲烷和乙烯的鉴别,题目难度不大,本题注意甲烷和乙烯在结构和性质上的异同.

练习册系列答案
相关题目
8.Na2O2晶体中含有的化学键有( )
| A. | 离子键、σ键 | B. | 极性键、离子键 | C. | 离子键 | D. | 离子键、π键 |
9.人们在研究金星大气成分时发现金星大气中有一种称为羰基硫(COS)的分子,其结构与CO2类似,羰基硫是一种与生命密切相关的物质,下列有关COS的推测不正确的是( )
| A. | COS分子是含有极性键的极性分子 | |
| B. | COS的电子式为: | |
| C. | COS的分子中所有原子满足8电子稳定结构 | |
| D. | COS分子中三个原子处于同一直线上 |
6.二甲苯的苯环上有一个氢原子被溴取代后的一溴代物有六种异构体,它们的熔点分别如下表所示.下列叙述正确的是( )
| 二甲苯一溴代物的熔点(℃) | 234 | 206 | 214 | 204 | 212 | 205 |
| 对应的二甲苯的熔点(℃) | 13 | -48 | -25 | -48 | -25 | -48 |
| A. | 点为234℃的是一溴代间二甲苯 | B. | 熔点为234℃的是一溴代邻二甲苯 | ||
| C. | 熔点为-48℃的是间二甲苯 | D. | 熔点为-25℃的是对二甲苯 |
13.下列说法中不正确的是( )
| A. | 浓硫酸能与灼热的木炭反应,生成二氧化碳和二氧化硫 | |
| B. | 浓硫酸具有吸水性,在实验室中常用作干燥剂 | |
| C. | 常温下,可以用铁质或铝质容器储存浓硫酸或浓硝酸 | |
| D. | 浓硫酸与铜反应产生的气体对环境无影响 |
3. 为研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
为研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
(1)实验①的目的是验证其他条件相同时,温度对化学反应速率的影响,实验中滴加FeCl3溶液的目的是催化剂,加快化学反应速率.
(2)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是③(填序号).
①加热5%H2O2溶液 ②分别加入5mL5%H2O2③加入1~2 滴1mol/L FeCl3溶液
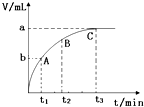
(3)某同学在50mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的即时反应速率最慢的是C.
 为研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
为研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中 | 试管A中不再产生气泡 试管B中产生的气泡量增大 |
| ② | 另取两支试管分别加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液 | 试管A、B中均未见气泡产生 |
(2)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是③(填序号).
①加热5%H2O2溶液 ②分别加入5mL5%H2O2③加入1~2 滴1mol/L FeCl3溶液
(3)某同学在50mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的即时反应速率最慢的是C.
10.下列有关醛的判断不正确的是( )
| A. | 用溴水检验CH2═CH-CHO中是否含有碳碳双键 | |
| B. | 1mol HCHO发生银镜反应最多生成4mol Ag | |
| C. | 乙醛能使高锰酸钾酸性溶液褪色 | |
| D. | 能发生银镜反应的有机物不一定是醛类 |
7.将一定量的N2和H2投入一密闭容器中,在一定条件下进行反应,测得有关数据如下:
根据以上相关数据回答问题:
(1)用H2表示该反应2s内的平均反应速率为0.6 mol•L-1•s-1.
(2)不能(填“能”或“不能”)确认该反应2s末已达化学平衡状态.
| N2(mol•L-1) | H2(mol•L-1) | NH3(mol•L-1) | |
| 起始时 | 3 | 3 | 0 |
| 2s末 | 2.6 | 1.8 | 0.8 |
(1)用H2表示该反应2s内的平均反应速率为0.6 mol•L-1•s-1.
(2)不能(填“能”或“不能”)确认该反应2s末已达化学平衡状态.
8.下列有关说法正确的是( )
| A. | H2SO4的酸性比HClO的酸性强,所以S的非金属性比Cl强 | |
| B. | Mg(OH)2是中强碱,Al(OH)3是两性氢氧化物,所以Al比Mg活泼 | |
| C. | H2S 300℃时开始分解,H2O 1000℃时开始分解,说明O的非金属性比S强 | |
| D. | Na和Mg与酸都能激烈反应放出氢气,故无法比较它们的金属性强弱 |