题目内容
10.下列有关醛的判断不正确的是( )| A. | 用溴水检验CH2═CH-CHO中是否含有碳碳双键 | |
| B. | 1mol HCHO发生银镜反应最多生成4mol Ag | |
| C. | 乙醛能使高锰酸钾酸性溶液褪色 | |
| D. | 能发生银镜反应的有机物不一定是醛类 |
分析 A、C=C、-CHO均能与溴水反应;
B、1mol HCHO中含2mol醛基;
C、醛基有很强的还原性;
D、只要含醛基就能发生银镜反应.
解答 解:A、C=C、-CHO均能与溴水反应,则用溴水不能检验CH2=CH-CHO中的碳碳双键,应先排除-CHO的干扰,不能实现,故A错误;
B、1mol HCHO中含2mol醛基,而1ml-CHO能反应生成2mol银,故1mol甲醛能生成4molAg,故B正确;
C、醛基有很强的还原性,能被强氧化剂高锰酸钾氧化,从而使高锰酸钾褪色,故C正确;
D、只要含醛基就能发生银镜反应,而含有醛基的不一定是醛类,如甲酸、甲酸某酯、甲酸盐以及葡萄糖和麦芽糖等均含醛基,能发生银镜反应,故D正确.
故选A.
点评 本题考查了官能团的检验和物质的结构特点,应注意的是1mol HCHO中含2mol醛基,故1mol甲醛能生成4molAg.

练习册系列答案
相关题目
20.下列有关稀有气体的描述不正确的是( )
①原子的最外层电子数都有8个 ②其原子与下周期第ⅠA族、ⅡA族的阳离子具有相同的电子层结构③有些稀有气体能跟某些物质反应 ④原子半径比同周期的元素的原子大.
①原子的最外层电子数都有8个 ②其原子与下周期第ⅠA族、ⅡA族的阳离子具有相同的电子层结构③有些稀有气体能跟某些物质反应 ④原子半径比同周期的元素的原子大.
| A. | 只有① | B. | ①和③ | C. | ①和② | D. | ②和④ |
1.锶(Sr)位于第五周期第ⅡA族,下来关于锶及其化合物的性质推断错误的是( )
| A. | Sr能与水反应,生成氢气 | |
| B. | Sr(OH)2具有两性 | |
| C. | SrSO4在水中溶解度很小 | |
| D. | SrCl2溶液和Na2CO3溶液能发生反应 |
18.区别CH4和C2H4的方法最好是( )
| A. | 通入溴水中观察溶液颜色的变化 | B. | 嗅闻它们的气味 | ||
| C. | 比较它们在水中的溶解度大小 | D. | 点燃它们后,观察火焰 |
5. Ⅰ.控制变量法是化学实验的一种常用方法.下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
Ⅰ.控制变量法是化学实验的一种常用方法.下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
(1)化学反应速率本质上是由反应物本身的性质决定的,但外界条件也会影响反应速率的大小.本实验中实验2和实验3表明温度对反应速率有影响,该因素对反应速率的具体影响是:其它条件相同时,温度越高反应速率越快.
(2)我们最好选取实验1、2和4(填3个实验序号)研究锌的形状对反应速率的影响.我们发现在其它条件相同时,反应物间的接触面积越大反应速率越快.
(3)若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快.原因是锌会置换出少量的金属铜,在该条件下构成了原电池,加快了反应速率.
(4)利用表中数据,可以求得:硫酸的物质的量浓度是2.0mol/L.
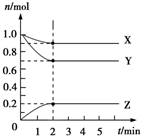
Ⅱ.某温度时,在5L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.请通过计算回答下列问题:
(5)反应开始至2min,Y的平均反应速率0.03mol/(L•min).
(6)分析有关数据,写出X、Y、Z的反应方程式X(g)+3Y(g)?2Z(g).
 Ⅰ.控制变量法是化学实验的一种常用方法.下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
Ⅰ.控制变量法是化学实验的一种常用方法.下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:| 序号 | 硫酸的体积/mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
| 1 | 50.0 | 2.0 | 薄片 | 25 | 100 | m1 |
| 2 | 50.0 | 2.0 | 颗粒 | 25 | 70 | m2 |
| 3 | 50.0 | 2.0 | 颗粒 | 35 | 35 | m3 |
| 4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
| 5 | 50.0 | 6.0 | 粉末 | 35 | 30 | m5 |
| 6 | 50.0 | 8.0 | 粉末 | 25 | t6 | 16.1 |
| 7 | 50.0 | 10.0 | 粉末 | 25 | t7 | 16.1 |
(2)我们最好选取实验1、2和4(填3个实验序号)研究锌的形状对反应速率的影响.我们发现在其它条件相同时,反应物间的接触面积越大反应速率越快.
(3)若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快.原因是锌会置换出少量的金属铜,在该条件下构成了原电池,加快了反应速率.
(4)利用表中数据,可以求得:硫酸的物质的量浓度是2.0mol/L.
Ⅱ.某温度时,在5L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.请通过计算回答下列问题:
(5)反应开始至2min,Y的平均反应速率0.03mol/(L•min).
(6)分析有关数据,写出X、Y、Z的反应方程式X(g)+3Y(g)?2Z(g).
15.下列气体中,有颜色的是( )
| A. | 氮气 | B. | 氯气 | C. | 二氧化碳 | D. | 二氧化硫 |
2.下列有关反应速率的说法正确的是( )
| A. | 用铁片和稀硫酸反应制氢气时,滴入几滴硫酸铜溶液可以加快反应速率 | |
| B. | 汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率变慢 | |
| C. | SO2的催化氧化反应是一个放热的反应,所以升高温度,反应速率变慢 | |
| D. | 100 mL 2 mol•L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 |
19.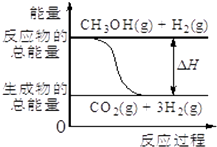 已知CH3OH(g)+H2O(g)=CO2(g)+3H2(g),该反应中的能量变化如图所示下列说法不正确的是( )
已知CH3OH(g)+H2O(g)=CO2(g)+3H2(g),该反应中的能量变化如图所示下列说法不正确的是( )
 已知CH3OH(g)+H2O(g)=CO2(g)+3H2(g),该反应中的能量变化如图所示下列说法不正确的是( )
已知CH3OH(g)+H2O(g)=CO2(g)+3H2(g),该反应中的能量变化如图所示下列说法不正确的是( )| A. | 该反应拆开反应物所有键所吸收的总能量小于形成生成物所放出的总能量 | |
| B. | 该反应是放热反应 | |
| C. | 该反应不能设计成原电池 | |
| D. | 该反应所有分子中各原子都以共价键相结合? |
20.下列物质在一定条件下能够与硫黄发生反应,且硫做还原剂的是( )
| A. | O2 | B. | Fe | C. | H2 | D. | Hg |