题目内容
10.63Li和73Li是锂的两种稳定同位素,在地质学和地球化学研究中有着广阔的应用前景.下列说法正确的是( )
| A. | 63Li和73Li是同一种核素 | B. | 63Li和73Li的中子数相同 | ||
| C. | 63Li和73Li的电子数相差1 | D. | 63Li和73Li的质子数相同 |
分析 根据原子符号中ZAX中的Z表示质子数,A表示质量数,质量数=质子数+中子数;同一核素是质子数相同,中子数也相同的原子.
解答 解:A.63Li和73Li的质子数都为3,质量数分别为7,6,中子数分别为7-3=4,6-3=3,不是同种核素,故A错误;
B.63Li和73Li的质子数都为3,质量数分别为7,6,中子数分别为7-3=4,6-3=3,故B错误;
C.63Li和73Li的质子数都为3,电子数也为3,故C错误;
D.63Li和73Li的质子数为3,故D正确;
故选D.
点评 本题主要考查了核素、原子符号的含义,掌握粒子间的数量关系式解题的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.短周期元素Q、W、Y原子序数依次增大,原子结构及性质如表所示:
(1)Y在元素周期表中的位置是第三周期ⅢA族.
(2)短周期中与W同主族元素的最高价氧化物的化学式SO3.
(3)元素Q的氧化物(溫室气体)、氢化物属于共价化合物(填“离子”、或“共价”),这些化合物分子内微粒间存在的作用力属于共价键(填离子键或共价键).
(4)单质Y可以发生如图所示的变化,回答:
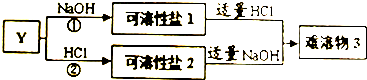
①写出反应①的离子方程式2Al+2H2O+2OH-=2AlO2-+3H2↑.
②下列化合物可替代Y发生如图所示的变化的是AC(填选项).
A、Y2O3 B、Y2(SO4)3 C、Y(OH)3 D、Y(NO3)3
③写出难溶物3的化学式Al(OH)3.
| 元素 | 结构与性质 |
| Q | Q元素的最高正、负价代数和为0.最高价氧化物为温室气体之一• |
| W | W是地壳中含量最高的非金属元素. |
| Y | Y所处的周期序数与主族序数相等,为地壳中含量最高的金属元素. |
(2)短周期中与W同主族元素的最高价氧化物的化学式SO3.
(3)元素Q的氧化物(溫室气体)、氢化物属于共价化合物(填“离子”、或“共价”),这些化合物分子内微粒间存在的作用力属于共价键(填离子键或共价键).
(4)单质Y可以发生如图所示的变化,回答:

①写出反应①的离子方程式2Al+2H2O+2OH-=2AlO2-+3H2↑.
②下列化合物可替代Y发生如图所示的变化的是AC(填选项).
A、Y2O3 B、Y2(SO4)3 C、Y(OH)3 D、Y(NO3)3
③写出难溶物3的化学式Al(OH)3.
18.把7.4g Na2CO3•10H2O和NaHCO3组成的混合物溶于水配成100mL溶液,测得溶液中钠离浓度为0.6mol/L.若把等质量的混合物加热至恒重,残留物的质量是( )
| A. | 3.18 g | B. | 2.12 g | C. | 4.22 g | D. | 5.28 g |
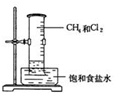
5.探究氯气是否具有漂白性实验如图:若关闭Ⅰ阀,打开Ⅱ阀,让一定量潮湿的氯气经过甲瓶后,进入乙瓶,乙瓶中布条不褪色.则甲瓶中所盛的试剂可能是:( )
①Na2SO3溶液 ②NaOH溶液 ③浓H2SO4 ④饱和NaCl溶液 ⑤KBr溶液.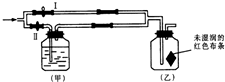
①Na2SO3溶液 ②NaOH溶液 ③浓H2SO4 ④饱和NaCl溶液 ⑤KBr溶液.

| A. | ②④ | B. | ②③⑤ | C. | ①②③⑤ | D. | ①②④ |
2.与纯水的电离相似,液氨中也存在着微弱的电离:2NH3?NH4++NH2-,据此判断以下叙述中不正确的是( )
| A. | 液氨中含有NH3、NH4+、NH2-微粒 | |
| B. | 其他条件不变,若增加液氨的量,电离平衡将正向移动 | |
| C. | 只要不加入其他物质,液氨中c(NH4+)=c(NH2-) | |
| D. | 一定温度下液氨中c(NH4+)•c(NH2-)是一个常数 |
19.如图为铁、铜水果电池装置示意图,下列说法正确的是( )
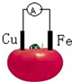

| A. | 铜片为负极 | B. | 铁片上发生还原反应 | ||
| C. | 电子由铁片沿导线流向铜极 | D. | 该装置将电能转变为化学能 |
20.下列关于硅及其氧化物的说法不正确的是( )
| A. | 硅是非金属元素,它的单质是灰黑色有金属光泽的固体 | |
| B. | 硅的导电性能介于导体和半导体之间,是良好的半导体材料 | |
| C. | 二氧化硅是酸性氧化物,不能和任何酸反应 | |
| D. | 信息高速公路的骨架----石英光导纤维的主要成份是二氧化硅 |
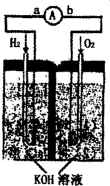 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的能力强,性质稳定.请回答: