题目内容
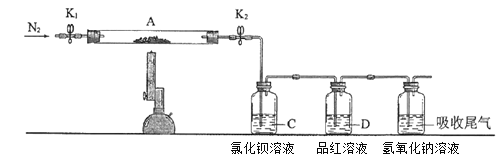
【题目】氯化铜、氯化亚铜是重要的化工原料,广泛用做有机合成催化剂。实验室可用如图所示装置,用还原铜粉和氯气来制备氯化铜。已知:氯化铜容易潮解。氯化亚铜微溶于水,不溶于稀盐酸和酒精。
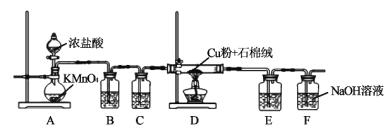
(1)装置A中发生反应的化学方程式为___。
(2)B装置的作用是___;C装置中的试剂是___;E装置的作用是___;F装置中可能发生的化学反应的离子方程式为___。
(3)当Cl2排尽空气后,加热D。装置D中的现象是___。
(4)另取CuCl2固体用于制备CuCl。将CuCl2固体溶解在适量蒸馏水中,并加入少量稀盐酸,然后向溶液中通入SO2气体并加热可得到CuCl白色沉淀,过滤、洗涤、干燥,即得CuCl晶体。
①制备CuCl反应的离子方程式为___;
②洗涤时,先用稀盐酸洗涤数次,后用酒精漂洗,用酒精漂洗的目的是___。
【答案】2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O 除去氯气中混有的氯化氢气体 浓硫酸 防止CuCl2潮解 Cl2+2OH-=Cl-+ClO-+H2O 产生棕黄色的烟 2Cu2++2Cl-+SO2+2H2O![]() 2CuCl↓+4H++SO42- 洗去CuCl沉淀表面的杂质,减少CuCl溶解损耗,有利于干燥
2CuCl↓+4H++SO42- 洗去CuCl沉淀表面的杂质,减少CuCl溶解损耗,有利于干燥
【解析】
装置A制备氯气,浓盐酸易挥发,所以氯气中含有少量氯化氢气体和水蒸气,需处理,否则会造成CuCl2的水解。CuCl2易潮解,E装置的作用得防止F中的水蒸气进入D装置而引起CuCl2水解。氯气有毒,不能直接排放到空气中。据此解答。
(1)KMnO4的氧化性强于MnO2,故在常温下能与浓盐酸反应产生Cl2,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。答案为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O;
(2)该反应为放热反应,浓盐酸易挥发,故生成的氯气中含有少量氯化氢气体,利用氯化氢极易溶于水,而氯气难溶于饱和食盐水,可用饱和食盐水将氯气中混有的氯化氢除去,故装置B的作用是除去氯气中混有的氯化氢气体。C装置中的试剂是浓硫酸,作用是干燥氯气。CuCl2易潮解,E装置中盛有浓硫酸,可防止F中的水蒸气进入D装置而引起CuCl2水解。氯气有毒,不能直接排放到空气中,F装置的作用是吸收未反应的氯气,反应的离子方程式为:Cl2+2OH- =Cl-+ClO-+H2O。答案为:除去氯气中混有的氯化氢气体;浓硫酸;防止CuCl2潮解;Cl2+2OH-=Cl-+ClO-+H2O;
(3)当Cl2排尽空气后,加热D,发生的反应为Cu+Cl2![]() CuCl2,现象是产生棕黄色的烟。答案为:产生棕黄色的烟;
CuCl2,现象是产生棕黄色的烟。答案为:产生棕黄色的烟;
(4)①CuCl2溶液与SO2发生氧化还原反应,生成CuCl沉淀和H2SO4,离子方程式为:2Cu2++2Cl-+SO2+2H2O![]() 2CuCl↓+4H++SO42-。答案为:2Cu2++2Cl-+SO2+2H2O
2CuCl↓+4H++SO42-。答案为:2Cu2++2Cl-+SO2+2H2O![]() 2CuCl↓+4H++SO42-;
2CuCl↓+4H++SO42-;
②CuCl微溶于水,不溶于稀盐酸和酒精,且酒精易挥发,故用酒精漂洗可洗去CuCl沉淀表面的杂质,减少CuCl溶解损耗,有利于干燥。答案为:洗去CuCl沉淀表面的杂质,减少CuCl溶解损耗,有利于干燥。

 全优点练单元计划系列答案
全优点练单元计划系列答案