题目内容
【题目】通常情况下,NCl3是一种油状液体,其分子空间构型与NH3相似,下列对NCl3和NH3的有关叙述正确的是( )
A. 分子中N—Cl键键长与CCl4分子中C—Cl键键长相等
B. NCl3分子是非极性分子
C. NBr3比NCl3易挥发
D. 在氨水中,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子,则NH3·H2O的结构式为![]()
【答案】D
【解析】
A、C的原子半径小于N原子半径,即N-Cl键长小于C-Cl键长,故A错误;
B、NH3为三角锥形,NCl3和NH3的空间构型相似,即NCl3空间构型为三角锥形,NCl3属于极性分子,故B错误;
C、NCl3和NBr3结构相似,NCl3相对分子质量小于NBr3,因此NCl3的熔沸点低于NBr3,故C错误;
D、NH3与H2O之间能形成分子间氢键,NH3·H2O能够电离出NH4+和OH-,因此NH3·H2O的结构式为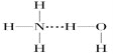 ,故D正确。
,故D正确。

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目