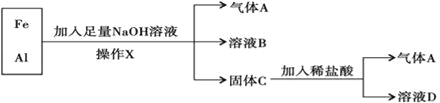
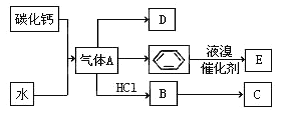
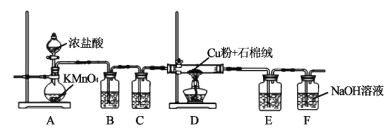
题目内容
【题目】某原电池装置如图所示,盐桥中装有琼脂与饱和K2SO4溶液,已知,氧化性:Cr2O72->Fe3+,下列叙述中不正确的是( )
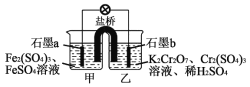
A.a电极为负极,b电极为正极
B.外电路中电子移动的方向:a极→导线→b极
C.电池工作时,盐桥中的K+移向甲烧杯
D.乙烧杯中发生的电极反应为:Cr2O72-+14H++6e-=2Cr3++7H2O
【答案】C
【解析】
A.氧化性:Cr2O72->Fe3+,所以该原电池反应中,Fe2+是还原剂,Cr2O72-是氧化剂,即a电极为原电池的负极,b电极为原电池的正极,A正确;
B.外电路中电子由负极移向正极,即由a极→导线→b极,B正确;
C.电池工作时,盐桥中的阳离子移向正极,即K+移向乙烧杯,C错误;
D.b电极为正极,正极得电子发生还原反应,电极反应为:Cr2O72-+14H++6e- =2Cr3++7H2O,D正确;
故选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目