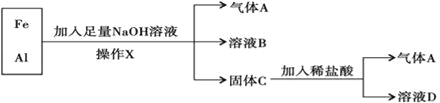
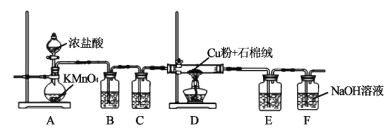
题目内容
【题目】根据所学化学反应原理,解决以下问题:
(1)请用离子方程式表示泡沫灭火器的工作原理___。
(2)请用离子方程式解释漂白粉和洁厕灵不能混合使用的原因___。
(3)难溶物ZnS可作为沉淀剂除去废水中的Cu2+,写出该过程的离子方程式___。
(4)用CO(g)还原80gFe2O3(s)生成Fe(s)和CO2(g),放热12.4kJ,请写出该反应的热化学方程式___。
(5)已知2CO(g)![]() CO2(g)+C(s),T=980K时,△H-T△S=0。在冶金工业中,以C为还原剂,温度高于980K时,C的氧化产物主要是___。
CO2(g)+C(s),T=980K时,△H-T△S=0。在冶金工业中,以C为还原剂,温度高于980K时,C的氧化产物主要是___。
【答案】Al3++3HCO3-=Al(OH)3↓+3CO2↑ ClO-+Cl-+2H+=Cl2↑+H2O ZnS(s)+Cu2+(aq)=CuS(s)+Zn2+(aq) 3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s) ΔH=-24.8kJ·mol-1 CO
【解析】
(1)泡沫灭火器的主要成分硫酸铝和碳酸氢钠,二者水解相互促进,工作原理用离子方程式表示:Al3++3HCO3-=Al(OH)3↓+3CO2↑。
(2)漂白粉次氯酸钙和洁厕灵稀盐酸不能混合使用的原因是因为二者发生氧化还原反应生成氯气:ClO-+Cl-+2H+=Cl2↑+H2O。
(3)难溶物ZnS可作为沉淀剂除去废水中的Cu2+,发生沉淀的转换,该过程的离子方程式为ZnS(s)+Cu2+(aq)=CuS(s)+Zn2+(aq)。
(4)80gFe2O3为0.5mol,则1mol氧化铁反应放热为24.8 kJ,该反应的热化学方程式3CO(g)+Fe2O3(g)=3CO2(g)+2Fe(s) ΔH=-24.8kJ·mol-1。
(5)已知2CO(g)![]() CO2(g)+C(s) △H<0,T=980K时,△H-T△S=0,因△H和△S值不变,且△S<0,体系温度低于980 K时,△H-T△S<0,反应能自发进行,当体系温度高于980 K时,△H-T△S>0,逆反应自发进行,故温度高于980 K时C的氧化产物主要是以CO为主。
CO2(g)+C(s) △H<0,T=980K时,△H-T△S=0,因△H和△S值不变,且△S<0,体系温度低于980 K时,△H-T△S<0,反应能自发进行,当体系温度高于980 K时,△H-T△S>0,逆反应自发进行,故温度高于980 K时C的氧化产物主要是以CO为主。

 名校课堂系列答案
名校课堂系列答案【题目】研究CO2与CH4反应使之转化为CO和H2,对减缓燃料危机和减少温室效应具有重要的意义。工业上CO2与CH4发生反应I:CH4(g)+CO2(g)=2CO(g)+2H2(g) △H1
在反应过程中还发生反应Ⅱ:H2(g)+CO2(g)=H2O(g)+CO(g)△H2=+41kJ/mol
(l)已知部分化学键的键能数据如下表所示:
化学键 | C—H | H—H | C=O |
|
键能(kJ/mol) | 413 | 436 | 803 | 1076 |
则△Hl =____kJ/mol,反应Ⅰ在一定条件下能够自发进行的原因是____,该反应工业生产适宜的温度和压强为____(填标号)。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
(2)工业上将CH4与CO2按物质的量1:1投料制取CO2和H2时,CH4和CO2的平衡转化率随温度变化关系如图所示。
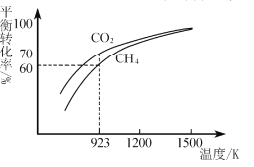
①923K时CO2的平衡转化率大于CH4的原因是________________________
②计算923K时反应II的化学平衡常数K=______(计算结果保留小数点后两位)。
③1200K以上CO2和CH4的平衡转化率趋于相等的原因可能是____。
(3)工业上CH4和CO2反应时通常会掺入O2发生反应
III: CH4+2O2=CO2+2H2O,掺人O2可消除反应产生的积碳和减小反应器的热负荷(单位时间内维持反应发生所需供给的热量),O2的进气量与反应的热负荷的关系如图所示。
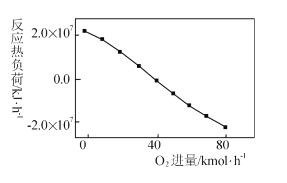
①随着O2进入量的增加,热负荷下降的原因是 ____。
②掺人O2可使CH4的平衡转化率____(填“增大”、“减小”或“不变”。下同),CO2的平衡转化率________