题目内容
16.下列说法正确的是( )| A. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| B. | NO可用于某些疾病的治疗 | |
| C. | NO2通入FeSO4溶液中始终无明显现象 | |
| D. | 汽车尾气的主要污染成分包括NO、CO和N2 |
分析 A、一氧化氮在空气中被氧化成二氧化氮;
B、NO的生物学特性有促使血红蛋白和肌球蛋白迅速强力抑制其血管舒张作用,则可用于心血管疾病的治疗;
C、二氧化氮与水反应生成硝酸,硝酸能将亚铁离子氧化成铁离子;
D、氮气无污染.
解答 解:A、一氧化氮在空气中不能稳定存在,被氧化成二氧化氮,故A错误;
B、NO的生物学特性有促使血红蛋白和肌球蛋白迅速强力抑制其血管舒张作用,则可用于心血管疾病的治疗,所以NO可用于某些疾病的治疗,故B正确;
C、二氧化氮与水反应生成硝酸,硝酸能将亚铁离子氧化成铁离子,溶液由浅绿色变成黄色,故C错误;
D、氮气无污染,故D错误;
故选B.
点评 本题考查氮及氮的化合物的性质,学生只要掌握氮元素及化合物的转化就可以迅速解题了,比较容易.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
4.图为实验室从海带中提取碘单质的流程示意图,判断下列说法错误的是( )
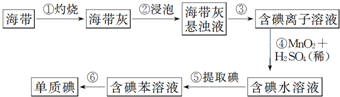

| A. | 步骤①需要用到蒸发皿 | B. | 步骤③需要过滤装置 | ||
| C. | 步骤⑤需要用到分液漏斗 | D. | 步骤⑥需要蒸馏装置 |
11.能在水溶液中大量共存的离子组是( )
| A. | H+ Fe3+ ClO-Cl- | B. | H+ SO32-Fe2+ NO3- | ||
| C. | Ag+ K+ Cl-SO42- | D. | K+ NH4+Cl- CO32- |
8.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 0.1mol的白磷(P4)或甲烷中所含的共价键数均为0.4NA | |
| B. | 标准状况下,一定量的铜与硝酸反应后生成22.4 L NO、NO2、N2O4的混合气体,则被还原的硝酸的分子数大于NA | |
| C. | 铁做电极电解食盐水,若阴极得到NA个电子,则阳极产生11.2L气体(标准状况下) | |
| D. | 标准状况下,2.24L Cl2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA |
11.有7种物质:①乙烷②乙烯③乙炔④苯⑤甲苯⑥溴乙烷⑦聚丙烯,其中既不能使酸性KMnO4溶液褪色,也不能与溴水因发生化学反应而使溴水褪色的是( )
| A. | ①②③⑤ | B. | ①④⑥⑦ | C. | ②④⑥⑦ | D. | ②③④⑤ |
 物,写出该化学反应方程式CH3CH2OH+CH2=CH2$\stackrel{一定条件下}{→}$CH3CH2OCH2CH3.
物,写出该化学反应方程式CH3CH2OH+CH2=CH2$\stackrel{一定条件下}{→}$CH3CH2OCH2CH3.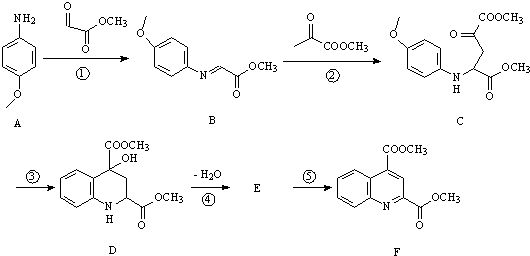

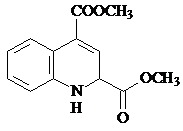 .
. 或
或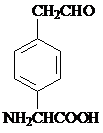 .
.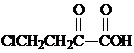 和苯、乙醇为原料,可合成
和苯、乙醇为原料,可合成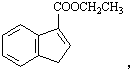 ,写出合成流程
,写出合成流程
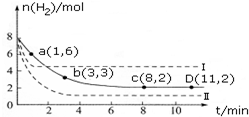 工业上研究利用CO2来生产甲醇燃料的方法,该方法的热化学方程式是:
工业上研究利用CO2来生产甲醇燃料的方法,该方法的热化学方程式是: