题目内容
4.图为实验室从海带中提取碘单质的流程示意图,判断下列说法错误的是( )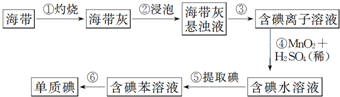
| A. | 步骤①需要用到蒸发皿 | B. | 步骤③需要过滤装置 | ||
| C. | 步骤⑤需要用到分液漏斗 | D. | 步骤⑥需要蒸馏装置 |
分析 由提取海带中的碘的实验流程可知,海带在坩埚中灼烧,然后溶解得到悬浊液,步骤③为过滤,得到含碘离子的溶液,④中发生MnO2+2I-+4H+=I2+Mn2++2H2O,得到含碘单质的溶液,⑤为萃取,⑥为蒸馏,以此来解答.
解答 解:由提取海带中的碘的实验流程可知,海带在坩埚中灼烧,然后溶解得到悬浊液,步骤③为过滤,得到含碘离子的溶液,④中发生MnO2+2I-+4H+=I2+Mn2++2H2O,得到含碘单质的溶液,⑤为萃取,⑥为蒸馏,
A.灼烧固体,应放在坩埚中,蒸发皿用于加热溶液,故A错误;
B.步骤③用于分离和固体和液体,得到含碘离子的溶液,为过滤操作,故B正确;
C.⑤为萃取,所用主要仪器是分液漏斗、烧杯,故C正确;
D.步骤⑥分离碘与苯,二者互溶,但沸点不同,则操作名称是蒸馏,故D正确.
故选A.
点评 本题以海带提碘为载体考查混合物分离提纯的综合应用,为高频考点,把握流程中的反应及混合物分离提纯方法为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
14.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 电解硫酸时,阴极产生1molH2时,阳极一定产生0.5molO2 | |
| B. | 盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5mol | |
| C. | 电解1mol熔融的Al2O3,能产生33.6L氧气、54.0g金属铝 | |
| D. | 工业用电解法进行粗铜精炼时,每转移1mol电子,阳极上就溶解0.5NA个铜原子 |
15.化学与能源开发、环境保护、资源利用等密切相关,下列说法正确的是( )
| A. | 硅酸钠的水溶液俗称水玻璃,可用作木材防火剂 | |
| B. | 开发核能、太阳能等新能,推广甲醇汽油,使用无磷洗涤剂都可直接降低碳排放 | |
| C. | 用聚合硫酸铁作为净水剂,该处理过程中仅发生了化学变化 | |
| D. | 汽车尾气中含有氮的氧化物,是汽油不完全燃烧造成的 |
12.下列离子方程式正确的是( )
| A. | 草酸可使酸性高锰酸钾溶液褪色,其离子方程式为:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O | |
| B. | 向NH4Al(SO4)2溶液中加入过量的Ba(OH)2稀溶液:NH4++Al3++2SO42-+2Ba2++5OH-=2BaSO4↓+NH3•H2O+AlO2-+2H2O | |
| C. | NaHSO3溶液与FeCl3反应的离子方程式:SO32-+2Fe3++H2O=SO42-+2Fe2++2H+ | |
| D. | NH4HCO3溶液中加入少量NaOH:NH4++OH-═NH3•H2O |
19.美国康乃尔大学的魏考克斯(C.Wilxox)所合成的一种有机分子,就像一尊释迦牟尼佛.因而称为释迦牟尼分子(所有原子在同一平面).有关该有机物分子的说法不正确的是( )

| A. | 该有机物属于苯的同系物 | |
| B. | 1mol该有机物完全燃烧需消耗25molO2 | |
| C. | 该有机物分子中含有21个碳原子 | |
| D. | 该有机物的一氯代物只有6种 |
9.下表所示的五种元素中,W、X、Y、Z为短周期元素,X元素的单质是空气中含量最多的成分.下列说法正确的是( )
| X | Y | ||
| W | Z | ||
| T |
| A. | X位于元素周期表中第二周期ⅤA族 | |
| B. | Y、Z形成氢化物的沸点更高是Z | |
| C. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| D. | 元素T与X的原子序数相差25 |
16.下列说法正确的是( )
| A. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| B. | NO可用于某些疾病的治疗 | |
| C. | NO2通入FeSO4溶液中始终无明显现象 | |
| D. | 汽车尾气的主要污染成分包括NO、CO和N2 |
13.下列说法正确的是( )
| A. | 乙烯使溴水或酸性高锰酸钾溶液褪色均属于加成反应 | |
| B. | 常温常压下环癸五烯 是一种易溶于水的无色气体 是一种易溶于水的无色气体 | |
| C. | 用酸性重铬酸钾溶液检验酒驾,发生的反应属于乙醇的氧化反应 | |
| D. | 等质量的乙烯和乙醇完全燃烧,消耗O2的物质的量相同 |
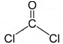 ,分子的立体构型是平面三角形.
,分子的立体构型是平面三角形.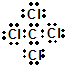 ,与CCl4互为等电子体的分子和离子分别有SiCl4和SO42-(各举一例,写化学式).
,与CCl4互为等电子体的分子和离子分别有SiCl4和SO42-(各举一例,写化学式).