题目内容
常温下某溶液中只含有Na+、H+、OH—、A—四种离子,下列说法正确的是
A.若溶质为NaA和HA,则一定存在c(A—)>c(Na+)>c(H+)>c(OH—)
B.若c(OH—)>c(H+),溶液中不可能存在c(Na+)>c(OH—)>c(A—)>c(H+)
C.溶液中可能存在c(Na+)>c(A—)>c(H+)>c(OH—)
D.若溶质为NaA,溶液中可能存在:c (OH—)=c(H+)+c(HA)
D
解析试题分析:溶液中必然存在如下电荷守恒式:c(Na+)+c(H+)=c(OH-)+c(A-),A项,因NaA和HA浓度未知,故无法确定具体离子浓度大小;B项,c(OH-)>c(H+),由电荷守恒可知c(Na+)>c(A-),若c(OH-)很大,可能出现c(OH-)>c(A-);C项,电荷不守恒;D项,是溶液中存在的质子守恒式。
考点:考查溶液中离子浓度大小比较,考查考生知识运用能力。

 名校课堂系列答案
名校课堂系列答案对水的电离平衡不产生影响的粒子是
| A.HCl | B.CH3COO- | C.Cl- | D.Fe3+ |
已知25℃时,Ka(HF)=3.6×10-4,Ksp(CaF2)=1.46×10-10。现向1L0.2mol·L-1HF溶液中加入1L0.2mol·L-1CaCl2溶液,则下列说法中,正确的是
| A.25℃时,0.lmol·L-1溶液中pH=l |
| B.Ksp(CaF2)随温度和浓度的变化而变化 |
| C.该体系中没有沉淀产生 |
| D.该体系中HF与CaC12反应产生沉淀 |
已知25℃时有关弱酸的电离平衡常数:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
25℃下,下列有关说法正确的是
A.浓度为0.1mol/L的HCN溶液中c(OH-)=10-13mol/L
B.物质的量浓度相同的稀酸溶液中KW:CH3COOH>H2CO3>HCN
C.物质的量浓度相同的三种钠盐溶液的pH:NaHCO3>NaCN>CH3COONa
D.浓度均为amol?L-1HCN溶液与NaOH溶液等体积混合充分反应后的溶液中(忽略体积的变化)c(H+)<c(OH-)<c(CN-)<0.5amol/L
难溶物BaSO4在水中的溶解平衡可表示为:BaSO4(s) Ba2+(aq)+SO42-(aq)。其溶度积常数Ksp=C(Ba2+)·C(SO42-),某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
Ba2+(aq)+SO42-(aq)。其溶度积常数Ksp=C(Ba2+)·C(SO42-),某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )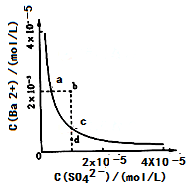
| A.D点无BaSO4沉淀生成 |
| B.加入Na2SO4可以使溶液由A点变到B点 |
| C.通过蒸发可以使溶液由D点变到C点 |
| D.A点对应的Ksp大于C点对应的Ksp |
常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。下列叙述正确的是 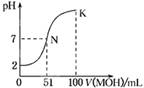
| A.HA为弱酸,MOH为强碱 |
| B.pH=7时,HA与MOH恰好完全反应 |
| C.在N点,c(A-)=c(M+) + c(MOH) |
| D.在K点,c(M+)>c(A-)>c(OH-)>c(H+) |
关于溶液的下列说法正确的是
| A.c(H+):c(OH-)=1:10-2的溶液中K+、Ba2+、ClO-、CO32-一定能大量存在 |
| B.水电离出来的c(H+)=10-13mol/L的溶液中K+、Cl-、NO3-、I-一定能大量存在 |
C.往0.1mol/LCH3COOH溶液中通人少量HCl,醋酸的电离平衡向逆反应方向移动,且溶液中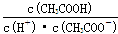 增大 增大 |
| D.等物质的量浓度的下列溶液:①H2CO3②Na2CO3③NaHCO3④(NH4)2CO3中c(CO32-)的大小关系为:②>④>③>① |
