题目内容
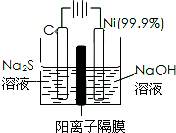 用电解的方法将硫化钠溶液氧化为多硫化物的研究具有重要的实际意义,将硫化物转变为多硫化物是电解法处理硫化氢废气的一个重要内容.如图,是电解产生多硫化物的实验装置:
用电解的方法将硫化钠溶液氧化为多硫化物的研究具有重要的实际意义,将硫化物转变为多硫化物是电解法处理硫化氢废气的一个重要内容.如图,是电解产生多硫化物的实验装置:①已知阳极的反应为:(x+1)S2-═SxS2-+2xe-,则阴极的电极反应式是:
②将Na2S?9H2O溶于水中配制硫化物溶液时,通常是在氮气气氛下溶解.其原因是(用离子反应方程式表示):
考点:原电池和电解池的工作原理
专题:电化学专题
分析:①电解时,阳极发生氧化反应,S2-失电子被氧化,阴极发生还原反应,H+得电子被还原生成氢气,结合电极方程式计算;
②Na2S?9H2O溶于水中配制硫化物溶液时,通常是在氮气气氛下溶解,原因是Na2S具有还原性,易被空气中的氧气氧化.
②Na2S?9H2O溶于水中配制硫化物溶液时,通常是在氮气气氛下溶解,原因是Na2S具有还原性,易被空气中的氧气氧化.
解答:
解:①电解时,阳极发生氧化反应,S2-失电子被氧化,阴极发生还原反应,H+得电子被还原生成氢气,电极方程式为2H++2e-=H2↑,当反应转移x mol电子时,可生成0.5xmolH2,体积为0.5xmol×22.4L/mol=11.2xL,
故答案为:2H++2e-=H2↑;11.2x L;
②Na2S?9H2O溶于水中配制硫化物溶液时,通常是在氮气气氛下溶解,原因是Na2S具有还原性,易被空气中的氧气氧化,反应的离子方程式为2S2-+O2+2H2O=2S↓+4OH-,
故答案为:2S2-+O2+2H2O=2S↓+4OH-.
故答案为:2H++2e-=H2↑;11.2x L;
②Na2S?9H2O溶于水中配制硫化物溶液时,通常是在氮气气氛下溶解,原因是Na2S具有还原性,易被空气中的氧气氧化,反应的离子方程式为2S2-+O2+2H2O=2S↓+4OH-,
故答案为:2S2-+O2+2H2O=2S↓+4OH-.
点评:本题考查较为综合,涉及电解池以及含硫化合物的性质等知识,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握题给信息以及电极方程式的书写,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列溶液中,含离子数目最多的是( )
| A、30mL 0.lmol/L的AlCl3 |
| B、10mL 0.2mol/L的CaCl2 |
| C、30mL 0.2mol/L的CH3COOH |
| D、40mL冰醋酸 |
下列关于钠的叙述中错误的是( )
| A、钠燃烧时发出黄色火焰,生成Na2O2 |
| B、钠投入CuSO4溶液中能生成红色的铜 |
| C、钠原子最外层有一个电子,具有强还原性 |
| D、钠与H2O反应能产生H2 |
设NA为阿佛加德罗常数的数值,下列说法正确的是( )
| A、等物质的量的H2和N2所含分子数均为NA |
| B、标准状况下,11.2L的己烷含有分子数为0.5NA |
| C、常温常压下,46g NO2含有原子数为3NA |
| D、1mol SiO2晶体中含NA个SiO2分子 |