题目内容
下列溶液中,含离子数目最多的是( )
| A、30mL 0.lmol/L的AlCl3 |
| B、10mL 0.2mol/L的CaCl2 |
| C、30mL 0.2mol/L的CH3COOH |
| D、40mL冰醋酸 |
考点:盐类水解的应用,弱电解质在水溶液中的电离平衡
专题:盐类的水解专题
分析:考虑物质的电离,所含溶质的离子数目最多即离子的物质的量最大,依据n=CV计算溶质物质的量,离子物质的量=溶质物质的量×化学式中离子数计算分析.
解答:
解:所含溶质的离子数目最多即离子的物质的量最大,依据n=CV计算溶质物质的量,离子物质的量=溶质物质的量×化学式中离子数计算分析.
A、30mL 0.lmol/L的AlCl3 ,溶质物质的量=0.030L×0.lmol/L=0.003mol,离子物质的量n(Al3+)=0.003mol,n(Cl-)=0.003mol×3=0.009mol,铝离子水解阳离子增多,离子总数大于0.012mol;
B、10mL 0.2mol/L的CaCl2 ,溶质物质的量=0.010L×0.2mol/L=0.002mol,离子物质的量n(Ca2+)=0.002mol,n(Cl-)=0.002mol×2=0.004mol,溶液中离子总数=0.006mol;
C、30mL 0.2mol/L的CH3COOH溶液中溶质物质的量=0.030L×0.2mol/L=0.006mol,醋酸是弱酸电离程度小,溶液中离子数远小于0.012mol;
D、40mL冰醋酸溶液中溶质是弱电解质,电离程度微弱,离子数少;
故上述分析A中离子数最大;
故选A.
A、30mL 0.lmol/L的AlCl3 ,溶质物质的量=0.030L×0.lmol/L=0.003mol,离子物质的量n(Al3+)=0.003mol,n(Cl-)=0.003mol×3=0.009mol,铝离子水解阳离子增多,离子总数大于0.012mol;
B、10mL 0.2mol/L的CaCl2 ,溶质物质的量=0.010L×0.2mol/L=0.002mol,离子物质的量n(Ca2+)=0.002mol,n(Cl-)=0.002mol×2=0.004mol,溶液中离子总数=0.006mol;
C、30mL 0.2mol/L的CH3COOH溶液中溶质物质的量=0.030L×0.2mol/L=0.006mol,醋酸是弱酸电离程度小,溶液中离子数远小于0.012mol;
D、40mL冰醋酸溶液中溶质是弱电解质,电离程度微弱,离子数少;
故上述分析A中离子数最大;
故选A.
点评:本题主要考查学生电解质的电离知识,结合离子数目来考查,增加了难度,注意弱电解质电离平衡的分析判断,题目难度中等.

练习册系列答案
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
对于利胆药-柳胺酚,下列说法正确的是( )


| A、1mol柳胺酚最多可以和2mol NaOH反应 |
| B、不发生取代反应 |
| C、可发生水解反应 |
| D、可与溴发生加成反应 |
下列结论中,正确的是( )
| A、摩尔是国际单位制的七个基本物理量之一 |
| B、0.012kg 12C约含有6.02×1023个碳原子 |
| C、1mol任何物质都含有6.02×1023个分子 |
| D、氢氧化钠的摩尔质量为40g |
下列说法中正确的是( )
| A、中和热的测定实验中需要用的主要玻璃仪器有:二只大小相同的烧杯、二只大小相同的量筒、温度计、环形玻璃搅拌捧 |
| B、可以用保温杯代替烧杯做有关中和热测定的实验 |
| C、在测定中和热的实验中,至少需要测定并记录的温度是3次 |
| D、测定中和热实验中,若所使用的稀NaOH溶液的物质的量稍大于稀盐酸,则会导致所测得的中和热数值偏高 |
2008年6月1日起,根据国务院要求所有超市、商场、集贸市场等商品零售场所实行塑料购物袋有偿使用.下列说法正确的是( )
| A、聚氯乙烯塑料属于烃类 |
| B、聚氯乙烯可以使酸性高锰酸钾溶液褪色 |
C、聚丙烯塑料的结构简式为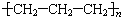 |
| D、聚丙烯是混合物 |
下列反应的离子方程式错误的是( )
| A、向碳酸氢钙溶液中加过量氢氧化钠Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- |
| B、等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3?H2O+H2O |
| C、氢氧化铝与足量盐酸反应 Al(OH)3+3H+═Al3++3H2O |
| D、过量CO2通入氢氧化钠溶液中 CO2+2OH-═CO32-+H2O |
 某有机物的结构简式如图,下列说法正确的是( )
某有机物的结构简式如图,下列说法正确的是( )| A、该有机物1 mol 能与3 mol H2在镍作催化剂条件下发生加成反应 |
| B、该有机物1 mol 能与1 mol H2在镍作催化剂条件下发生加成反应 |
| C、该有机物能与NaHCO3反应放出CO2 |
| D、该有机物在一定条件下能发生银镜反应 |
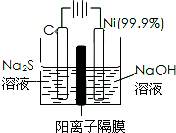 用电解的方法将硫化钠溶液氧化为多硫化物的研究具有重要的实际意义,将硫化物转变为多硫化物是电解法处理硫化氢废气的一个重要内容.如图,是电解产生多硫化物的实验装置:
用电解的方法将硫化钠溶液氧化为多硫化物的研究具有重要的实际意义,将硫化物转变为多硫化物是电解法处理硫化氢废气的一个重要内容.如图,是电解产生多硫化物的实验装置: