题目内容
【题目】25℃,用0.100mol·L-1的NaOH溶液分别滴定20.00mL0.100mol·L-1的盐酸和0.100mol·L-1的醋酸,得到如图所示滴定曲线:
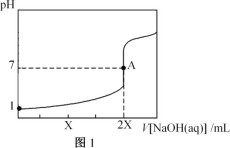
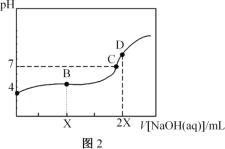
下列说法不正确的是( )
A.图1表示的是滴定盐酸的曲线
B.图2滴定应选用甲基橙做指示剂
C.图中A、D点水的电离程度:A<D
D.图2中B点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
【答案】B
【解析】
A.根据图示信息,滴定开始时,0.100mol/L的盐酸pH为1,故图1是盐酸的滴定曲线,A正确;
B.根据图示信息,图2是氢氧化钠滴入醋酸中,反应生成醋酸钠,溶液呈碱性,只能选择酚酞作指示剂,B错误;
C.达到图中A、D点时,消耗的氢氧化钠的物质的量是相等的,生成物是氯化钠和醋酸钠,醋酸钠水解促进水的电离,故水的电离程度:A<D,C正确;
D.图2中B点溶质成分为醋酸钠和醋酸,且物质的量为1:1,溶液呈酸性,说明醋酸的电离程度大于醋酸根的水解程度,所以溶液中浓度大小为c(CH3COO-)>c(Na+)>c(H+)>c(OH-),D正确;
故选B。

【题目】某酸性工业废水中含有K2Cr2O7。光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应堆起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,做对比实验。请完成以下实验设计表(表中不要留空格)。
实验序号 | 初始pH | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
① | 4.0 | 60.0 | 10.0 | 30.0 |
② | 5.0 | 60.0 | 10.0 | 30.0 |
③ | 5.0 | 60.0 | ______ | ______ |
测得实验①和②溶液中Cr2O72-的浓度随时间变化关系如图所示。
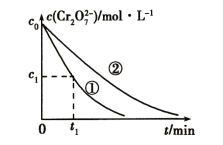
(2)上述反应的离子方程式为_______。
(3)对比实验①和②的结果可得出结论______。实验①中0~t1时间段反应速率v(Cr3+)=_____(用代数式表示)。
(4)该课题组对铁明矾[Al2Fe(SO4)4·24H2O]中起催化作用的成分提出如了下假设,请你完成假设二:
假设一:Fe2+起催化作用;
假设二:___________;
······
【题目】电解质的水溶液中存在电离平衡。
(1)醋酸是常见的弱酸。
①醋酸在水溶液中的电离方程式为____________。
②下列方法中,可以使醋酸溶液中CH3COOH电离程度增大的是_______(填字母序号)。
a 滴加少量浓盐酸 b 微热溶液 c 加水稀释 d 加入少量醋酸钠晶体
(2)下表为某同学所测25℃时,甲、乙两种溶液的pH。
甲 | 乙 | |
pH | 11 | 11 |
溶液 | 氨水 | 氢氧化钠溶液 |
①甲溶液中的c(OH-) =___________mol/L。
②25℃时,等体积的甲、乙两溶液与等浓度的盐酸反应,消耗的盐酸体积:甲_____乙。
③甲、乙溶液均加水稀释10倍后,所得溶液的pH:甲_____乙。
(3)已知多元弱酸在水溶液中的电离是分步进行的,且第一步的电离程度大于第二步的电离程度,第二步的电离程度远大于第三步的电离程度……今有HA、H2B、H3C三种弱酸,根据“较强酸 + 较弱酸盐 = 较强酸盐 + 较弱酸”的反应规律,它们之间能发生下列反应:
a.HA + HC2-(少量) = A-+ H2C-
b.H2B(少量) + 2A- = B2- + 2HA
c.H2B(少量) + H2C- = HB-+ H3C
回答下列问题:
①相同条件下,HA、H2B、H3C三种酸中,酸性最强的是_____________。
②下列反应的离子方程式正确的是____________。
A.H3C +3A- = 3HA + C3- B.HB- +A- = HA + B2-
③完成下列反应的离子方程式:
a.H3C + OH-(过量)——__________________;b.HA(过量) + C3- ——_____________________。