题目内容
【题目】(1)亚硝酸钠(NaNO2)外观酷似食盐,但它是一种有毒的物质。误食亚硝酸钠会使人体血液中的Fe2+转化为Fe3+而引起中毒,服用维生素C可使Fe3+转化为Fe2+,从而达到解毒的目的。转化过程可表示为:Fe2+![]() Fe3+,转化1中,氧化剂是____,转化2中,维生素C表现____性。
Fe3+,转化1中,氧化剂是____,转化2中,维生素C表现____性。
(2)在①盐酸、②浓硝酸、③氨水、④稀硫酸、⑤氢氧化钠溶液五种物质中,可用于除去Al表面的铜镀层的是_____(填序号);实验室常用硫酸铝溶液和____(填序号)反应制取氢氧化铝,反应的离子反应方程式是_____。
(3)把一定量铜粉投入氯化铁、氯化铜的混合溶液中,完全反应后,所得溶液中Cu2+、Fe2+和Fe3+三种离子的浓度恰好相等。则原溶液中的Fe3+和Cu2+的物质的量之比为_____。
【答案】NaNO2(或亚硝酸钠) 还原 ② ③ Al3++3NH3·H2O=Al(OH)3↓+3NH4+ 4:1
【解析】
(1)转化1中,Fe元素化合价由+2价变为+3价,转化2中,Fe元素化合价由+3价变为+2价;
(2)除去Al表面的铜镀层选择的试剂应能与铜反应而除去,并保证铝不得反应;氢氧化铝是两性氢氧化物,能溶于强酸强碱,不溶于弱酸弱碱;
(3)由方程式结合溶液中Cu2+、Fe2+和Fe3+三种离子的浓度恰好相等建立关系式求解。
(1)转化1中,Fe元素化合价由+2价变为+3价,则亚铁离子被氧化而作还原剂,亚硝酸钠作氧化剂;转化2中,Fe元素化合价由+3价变为+2价,铁元素得电子而作氧化剂,则维生素C作还原剂,维生素C体现还原性,故答案为:NaNO2(或亚硝酸钠);还原;
(2)除去Al表面的铜镀层选择的试剂应能与铜反应而除去,并保证铝不得反应。根据金属活动顺序表可知,铝能和盐酸、稀硫酸反应,铜与盐酸、稀硫酸不反应,铝和氢氧化钠溶液反应,铜和氢氧化钠溶液不反应,铝在浓硝酸中发生钝化,铜与浓硝酸反应,则选择的试剂为浓硝酸;氢氧化铝是两性氢氧化物,能溶于强酸强碱,不溶于弱酸弱碱,则实验室常用硫酸铝溶液和氨水反应制备氢氧化铝,反应的离子方程式为Al3++3NH3·H2O=Al(OH)3↓+3NH4+,故答案为:②;③。Al3++3NH3·H2O=Al(OH)3↓+3NH4+;
(3)由题意可知,把一定量铜粉投入氯化铁、氯化铜的混合溶液中,铜粉与部分氯化铁溶液反应生成氯化亚铁和氯化铜,反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+,设原溶液中的Fe3+和Cu2+的物质的量分别为x、y,生成Fe2+的物质的量为2a,由方程式结合溶液中Cu2+、Fe2+和Fe3+三种离子的浓度恰好相等可得(y+a)=2a=(x—2a),解得y=a、x=4a,x:y=4:1,故答案为:4:1.

【题目】![]() 和
和![]() 既是温室气体又是丰富的碳基资源。甲烷与二氧化碳重整反应是制合成气(
既是温室气体又是丰富的碳基资源。甲烷与二氧化碳重整反应是制合成气(![]() )的有效途径之一。合成气可用于二甲醚合成、羰基合成、费托合成等。因此,具有较好的市场前景。
)的有效途径之一。合成气可用于二甲醚合成、羰基合成、费托合成等。因此,具有较好的市场前景。
(1)已知在![]() 、298K条件下,各物质燃烧热数据如下表:
、298K条件下,各物质燃烧热数据如下表:
物质(g) |
|
|
|
|
燃烧热( | -890.0 | -283.0 | -285.0 | 0 |
则甲烷与二氧化碳重整反应制合成气的热化学方程式为:________________;
(2)在T℃时,向容积为2L的刚性容器中充入![]()
![]() 和
和![]()
![]() 。反应体系中
。反应体系中![]() 的物质的量随时间变化关系如下表:
的物质的量随时间变化关系如下表:
时间/min | 0 | 20 | 50 | 100 | |
| 0.5 | 0.48 | 0.25 | 0.25 | 0.25 |
①20min时,![]() ________
________![]() ;当反应进行到60min时,
;当反应进行到60min时,![]() ________20min时
________20min时![]() 的大小关系(填“<”、“=”或“>”);反应进行到60min时,下列能够提高平衡时合成气产率的措施有:_______________________。
的大小关系(填“<”、“=”或“>”);反应进行到60min时,下列能够提高平衡时合成气产率的措施有:_______________________。
A.将反应时间延长至150min B.移除一部分合成气
C.适当提高反应升高温度 D.改用高效催化剂
②反应进行到下列各图的p点时,能够说明该反应达到平衡状态的是:___________。
A. B.
B. C.
C.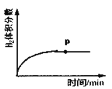 D.
D.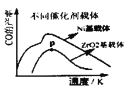
③已知:p(H2)、p(CO)、p(CH4)和p(CO2)为各组分的平衡分压(气体分压p=气体总压p总×体积分数),p总为平衡总压。若开始测得反应体系的压强为3.0Mpa,则合成气反应达到平衡状态时Kp=________。(结果保留一位小数)
(3)由于原料气的![]() 比较高,催化剂易结焦,特别是高温反应时积碳严重,影响了此过程大规模工业化的应用。某科研小组研究了Sr助剂对10%
比较高,催化剂易结焦,特别是高温反应时积碳严重,影响了此过程大规模工业化的应用。某科研小组研究了Sr助剂对10%![]() 催化剂性能的影响如表1所示,请判断催化剂上Sr助剂的最佳质量含量为________(横坐标表示Sr助剂的质量含量),判断的理由是________________(写出两点)
催化剂性能的影响如表1所示,请判断催化剂上Sr助剂的最佳质量含量为________(横坐标表示Sr助剂的质量含量),判断的理由是________________(写出两点)

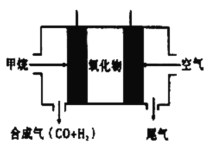
(4)如图所示,以![]() 为燃料气,高温电化学法制备合成气的发电系统中,
为燃料气,高温电化学法制备合成气的发电系统中,![]() 在电场作用下,通过氧化物电解质中氧空位迁移到负极,与
在电场作用下,通过氧化物电解质中氧空位迁移到负极,与![]() 发生氧化还原反应。试用电极反应方程式表示负极发生反应的总过程:___________________________________。
发生氧化还原反应。试用电极反应方程式表示负极发生反应的总过程:___________________________________。