题目内容
【题目】接触法制硫酸工艺中,其主反应如下:
2SO2(g) + O2(g) ![]() 2SO3(g)
2SO3(g) ![]() H=-197 kJ/mol
H=-197 kJ/mol
下列说法正确的是
A. 因为反应放热,所以该反应不需要加热即能快速反应
B. 增大O2的浓度可以提高反应速率和SO2的转化率
C. 反应450℃时的平衡常数小于500℃时的平衡常数
D. 恒温下缩小容器容积,使Q > K
【答案】B
【解析】
A.反应是吸热还是放热与是否加热无关,该反应不加热不能快速反应,故A错误;
B. 增大O2的浓度可以提高反应速率,且平衡正向移动,则SO2的转化率增大,故B正确;
C.该反应为放热反应,升温平衡逆向移动,则反应450℃时的平衡常数大于500℃时的平衡常数,故C错误;
D. 恒温下缩小容器容积,相当于增大压强,平衡正向移动,使Q < K,故D错误;
故选B。

【题目】有机物A是一种纯净的无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 | 解释或实验结论 |
(1)称取A物质18.0g,升温使其汽化,测其密度是相同条 件下H2的45倍。 | A的相对分子质量为____ |
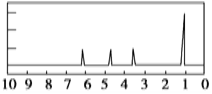
(2)A的核磁共振氢谱如下图:
| A中含有____种氢原子且吸收峰面积比为____ |
(3)另取A18.0g与足量的NaHCO3粉末反应,生成0.2mol CO2,若与足量钠反应则生成0.2molH2。 | A中所含官能团名称为______________ |
(4)将此18.0gA在足量O2中充分燃烧,并使其产物依次 缓缓通过浓硫酸、碱石灰,发现两者依次增重10.8g和26.4g。 | A的分子式___________ |
(5)综上所述,A的结构简式为____ | |
【题目】由下列实验及现象能推出相应结论的是( )
实验 | 实验现象 | 实验结论 | |
A | 用洁净的铂丝蘸取少量溶液在酒精灯外焰上灼烧 | 火焰呈黄色 | 该溶液中一定含有Na+,无K+ |
B | 向某溶液中加入BaCl2溶液 | 有白色沉淀 | 该溶液中一定有SO |
C | 将某气体通入品红溶液 | 红色褪去 | 该气体一定是SO2 |
D | 将一小块用砂纸打磨过的铝箔在酒精灯上加热 | 熔化的液态铝不会滴落 | 表面生成的Al2O3薄膜熔点较高 |
A.AB.BC.CD.D