题目内容
17.短周期A、B、C、D、E、F六种元素,它们的原子序数由A到F 依次增大.在周期表中,A的原子半径最小.B元素的原子最外层电子数是内层电子数的两倍,C为地壳中含量最多的元素,D是原子半径最大的短周期主族元素,D单质燃烧时呈现黄色火焰,D的单质在高温下与C的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物.D与F形成的离子化合物DF是常用的调味品.试根据以上叙述回答:(1)元素名称:B、碳,D、钠.
(2)E在周期表中的位置:第三周期第ⅥA族.
(3)F离子结构示意图:
 .
.(4)A、B组成的最简单有机化合物的名称是甲烷.
(5)写出BC2与过量氢氧化钠溶液反应的离子方程式CO2+2OH-=CO32-+H2O.
(6)C单质与D单质发生反应的产物有Na2O、Na2O2(填化学式).C、D组成的一种化合物与水发生化合反应的化学方程式为:Na2O+H2O=2NaOH.
(7)能说明E的非金属性比F的非金属性弱(填“强”或“弱”)的事实是氯气能从硫化钠溶液中置换出硫(举一例).
分析 短周期A、B、C、D、E、F六种元素,它们的原子序数由A到F依次增大,在周期表中,A的原子半径最小,则A为氢元素,B元素的原子最外层电子数是内层电子数的两倍,则B为碳元素,C为地壳中含量最多的元素,则C为氧元素,D是原子半径最大的短周期主族元素,D单质燃烧时呈现黄色火焰,则D为钠元素,D的单质在高温下与C的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物,则E为硫元素,D与F形成的化合物DF是常用的调味品,则F为氯元素,据此答题.
解答 解:短周期元素A、B、C、D、E、F六种元素,它们的原子序数由A到F依次增大,在周期表中,A的原子半径最小,则A为氢元素,B元素的原子最外层电子数是内层电子数的两倍,则B为碳元素,C为地壳中含量最多的元素,则C为氧元素,D是原子半径最大的短周期主族元素,D单质燃烧时呈现黄色火焰,则D为钠元素,D的单质在高温下与C的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物,则E为硫元素,D与F形成的化合物DF是常用的调味品,则F为氯元素.
(1)根据上面的分析可知,B为碳元素,D为钠元素,故答案为:碳;钠;
(2)E为硫元素,E在元素周期表中的位置第三周期第ⅥA族,故答案为:第三周期第ⅥA族;
(3)F为氯元素,Cl-离子结构示意图为 ,故答案为:
,故答案为: ;
;
(4)A为氢元素,B为碳元素,A、B组成的最简单化合物的名称是甲烷,故答案为:甲烷;
(5)CO2与过量氢氧化钠溶液反应的离子方程式:CO2+2OH-=CO32-+H2O,故答案为:CO2+2OH-=CO32-+H2O;
(6)C单质与D单质发生反应的产物有Na2O、Na2O2.C、D组成的一种化合物与水发生化合反应的化学方程式为:Na2O+H2O=2NaOH,
故答案为:Na2O、Na2O2;Na2O+H2O=2NaOH;
(7)E为硫元素,F为氯元素,根据元素周期律可知硫的非金属性弱于氯,能说明这一事实的是氯气能从硫化钠溶液中置换出硫,
故答案为:弱;氯气能从硫化钠溶液中置换出硫.
点评 本题考查结构性质位置关系应用,难度不大,明确元素种类是解题关键,注意掌握金属性、非金属性强弱比较实验事实,有利于基础知识的巩固.

 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案| A. | 原子核内有10个中子的氧原子:188188O | |
| B. | NH4Cl的电子式为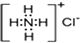 | |
| C. | 羟基的电子式: | |
| D. | 乙醇的分子式:CH3CH2OH |
( )
| A. | 芥子气不是烃的衍生物 | |
| B. | 芥子气可以和硝酸银溶液反应生成氯化银沉淀 | |
| C. | S2Cl2中有极性键和非极性键 | |
| D. | NaOH溶液解毒原理是酸碱中和反应 |
| A. | 利用太阳能、潮汐能、风力发电,可以获取清洁能源 | |
| B. | 常在包装袋内放入生石灰以防止月饼等富脂食品氧化变质 | |
| C. | 利用可降解的“玉米塑料”生产一次性饭盒,可防止白色污染 | |
| D. | 采用纳米二氧化钛光触媒技术可将汽车尾气中的NO和CO转化为无害气体 |

 (该反应不需要条件就迅速转化)
(该反应不需要条件就迅速转化) .
.
 +H2O.
+H2O. 在化学课上,围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀.然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体.请回答:
在化学课上,围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀.然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体.请回答: (1)氢能源是21世纪极具有发展前景的新能源之一,它既是绿色能源,又可循环使用.请在下图的每个空格中填上循环过程中反应物和生成物的分子式,以完成理想的氢能源循环体系图(循环中接受太阳能的物质在自然界中广泛存在):①H2O,②H2和O2.从能量转换的角度看,过程Ⅱ应是化学能转化为电能.
(1)氢能源是21世纪极具有发展前景的新能源之一,它既是绿色能源,又可循环使用.请在下图的每个空格中填上循环过程中反应物和生成物的分子式,以完成理想的氢能源循环体系图(循环中接受太阳能的物质在自然界中广泛存在):①H2O,②H2和O2.从能量转换的角度看,过程Ⅱ应是化学能转化为电能.