题目内容
12.今年是世界反法西斯战争暨中国人民抗日战争胜利70周年.二战期间日本是在战场上唯一大量使用毒气弹的国家.芥子气〔(ClCH2CH2)2S〕是其中一种毒气,即使嗅觉不能感受的极低浓度也会对人造成伤害,可用NaOH溶液解毒.芥子气可用以下方法制备:2CH2=CH2+S2Cl2→(ClCH2CH2)2S+S.下列有关说法正确的是( )
| A. | 芥子气不是烃的衍生物 | |
| B. | 芥子气可以和硝酸银溶液反应生成氯化银沉淀 | |
| C. | S2Cl2中有极性键和非极性键 | |
| D. | NaOH溶液解毒原理是酸碱中和反应 |
分析 A.含有S、Cl等元素,为烃的衍生物;
B.为非电解质,不能电离;
C.同种非金属之间形成非极性键,不同非金属之间形成极性键;
D.(ClCH2CH2)2S在氢氧化钠中发生卤代烃的水解反应.
解答 解:A.芥子气含有S、Cl等元素,为烃的衍生物,故A错误;
B.为非电解质,不能电离,加入硝酸银,不能生成沉淀,故B错误;
C.同种非金属之间形成非极性键,不同非金属之间形成极性键,则S2Cl2中有S-Cl极性键和S-S非极性键,故C正确;
D.(ClCH2CH2)2S在氢氧化钠中发生卤代烃的水解反应,所以NaOH溶液解毒原理是发生卤代烃的水解反应,故D错误.
故选C.
点评 本题考查较为综合,涉及有机物的结构和性质、共价键以及电解质的电离等知识,为高频考点,侧重基本概念、基本理论的考查,注意相关知识的积累,难度不大.

练习册系列答案
相关题目
2.碘131是碘元素的一种放射性核素.下列关于${\;}_{53}^{131}$I的说法正确的是( )
| A. | 质子数为78 | B. | 中子数为53 | C. | 质量数为131 | D. | 核外电子数为78 |
7.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 22.4LCO和CO2的混合气体中所含的碳原子数一定是NA | |
| B. | 标况下,22.4L氦气所含原子数为2NA | |
| C. | 常温常压下,32gO2和32gO3所含氧原子数都是2NA | |
| D. | 常温下5.6g铁投入到足量浓硝酸中反应,转移电子数为0.3NA |
4.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,15g乙烷分子中含有的碳氢键数目为3NA | |
| B. | 标准状态下,22.4L的苯的分子数为NA | |
| C. | 通常状态下,1.7g的NH3中含有中子数为NA | |
| D. | 23gNa放入水中反应后共失去电子2NA |
1.下列离子在水溶液中一定能大量共存的是( )
| A. | K+ NH4+ HCO3- OH- | B. | Fe2+ H+ NO3- SO42- | ||
| C. | Na+ Cu2+ SO42- NO3- | D. | Al3+ Ba2+ CO32- Cl- |


 +2CH3COOH$→_{△}^{浓硫酸}$
+2CH3COOH$→_{△}^{浓硫酸}$ +2H2O.
+2H2O. ,
, ,
, .
.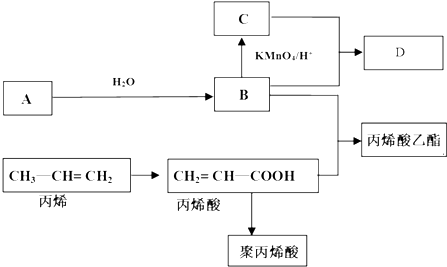
 CH2=CH-COOC2H5+H2O反应类型:酯化反应或取代反应
CH2=CH-COOC2H5+H2O反应类型:酯化反应或取代反应 .
.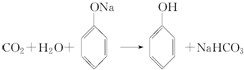
 +H2O.
+H2O.