题目内容
3.A、B、C、D、E均为氯的含氧化合物,我们不了解它们的分子式(或化学式),但知道它们在一定条件下具有如下的转化关系(未配平):①B+H2O $\stackrel{电解}{→}$ C+H2↑ ②A→B+NaCl ③E+NaOH→B+C+H2O ④D+NaOH→A+B+H2O
这五种化合物中含氯的化合价由高到低的顺序为( )
| A. | C、B、E、D、A | B. | B、D、A、C、E | C. | C、D、E、A、B | D. | C、E、B、D、A |
分析 A、B、C、D、E均为氯的含氧化合物,根据氧化还原反应中Cl元素的化合价升降来分析解答.
解答 解:①B+H2O $\stackrel{电解}{→}$ C+H2↑,H元素的化合价降低,则Cl元素的化合价升高,所以Cl元素的化合价为C>B,
②A→B+NaCl中,NaCl中Cl元素为-1价,则Cl元素的化合价为B>A>-1,
③E+NaOH→B+C+H2O中,结合①可知Cl元素的化合价为C>E>B,
④D+NaOH→A+B+H2O中,结合②可知,Cl元素的化合价为B>D>A,
所以五种化合物中氯的化合价由高到低的顺序为CEBDA,
故选D.
点评 本题考查氧化还原反应,明确氧化还原反应中元素的化合价变化是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
13.有机物分子中,若有1个碳原子用4个单键与4个互不相同的原子或原子团相连,这样的碳原子称为“手性碳”.若烯烃 分子中含有手性碳,该烯烃的一个分子中至少含有的碳原子数是( )
| A. | 5 | B. | 6 | C. | 7 | D. | 8 |
14.常温下(I)100mL0.1mol/L的NaA溶液中的离子总物质的量为X,(Ⅱ)100mL 0.1mol/L的NaB溶液中的离子总物质的量为Y.下列推断正确的是( )
| A. | 若X>Y,则酸性:HA>HB | |
| B. | 若X=Y,则HB一定是强酸 | |
| C. | 若酸性:HA<HB,则X和Y关系不确定 | |
| D. | 若由水电离出的H+的浓度:(I)>(Ⅱ),则是X>Y |
1.下列各物质中,互为同系物的是( )
| A. | 丁烷和2,2-二甲基丙烷 | B. |  和 和 | ||
| C. | CH2=CH-CH=CH2和CH3-CH2-C≡CH | D. |  和 和 |
 ,其所含有的官能团有(写结构简式)-$\underset{\stackrel{\;}{C}}{|}=O$、-OH、C=C、-O-.
,其所含有的官能团有(写结构简式)-$\underset{\stackrel{\;}{C}}{|}=O$、-OH、C=C、-O-. .这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究成果.L-多巴分子中所含的官能团的名称是羟基、氨基和羧基.
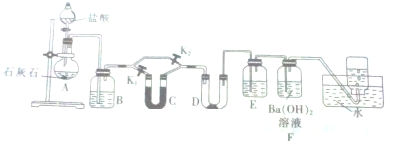
.这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究成果.L-多巴分子中所含的官能团的名称是羟基、氨基和羧基. 如图是实验室制备SO2并验证SO2某些性质的装置图.
如图是实验室制备SO2并验证SO2某些性质的装置图.