题目内容
下列离子方程式书写正确的是( )
| A、用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | ||||
| B、利用腐蚀法制作印刷线路析:Fe3++Cu═Fe2++Cu2+ | ||||
C、用铜电极电解硫酸铜溶液:2Cu2++2H2O
| ||||
| D、硫酸氧钠溶液中加入氢氧化钡溶液至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A、醋酸是弱酸;
B、从电荷是否失衡角度来分析;
C、用铜电极电解硫酸铜溶液时,阳极的铜电极会参与反应;
D、根据硫酸氧钠溶液中加入氢氧化钡溶液至中性来分析反应物的比例.
B、从电荷是否失衡角度来分析;
C、用铜电极电解硫酸铜溶液时,阳极的铜电极会参与反应;
D、根据硫酸氧钠溶液中加入氢氧化钡溶液至中性来分析反应物的比例.
解答:
解:A、用醋酸除去水垢的化学方程式:CaCO3+2CH3COOH═(CH3COO)2Ca+H2O+CO2↑,醋酸是弱酸,不能拆,故离子方程式为:CaCO3+2CH3COOH═CH3COO-+Ca2++H2O+CO2↑,故A错误;
B、此离子方程式电荷不守恒,正确的离子方程式为:2Fe3++Cu═2Fe2++Cu2+,故B错误;
C、用铜电极电解硫酸铜溶液时,阳极上是铜电极放电:Cu-2e-=Cu2+,阴极上是Cu2+放电:Cu2++2e-=Cu,故C错误;
D、根据硫酸氧钠溶液中加入氢氧化钡溶液至中性可知两者的物质的量之比为2:1,从而化学方程式为:2NaHSO4 +Ba(OH)2=2H2O+BaSO4↓+Na2SO4,故离子方程式为:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D正确.
B、此离子方程式电荷不守恒,正确的离子方程式为:2Fe3++Cu═2Fe2++Cu2+,故B错误;
C、用铜电极电解硫酸铜溶液时,阳极上是铜电极放电:Cu-2e-=Cu2+,阴极上是Cu2+放电:Cu2++2e-=Cu,故C错误;
D、根据硫酸氧钠溶液中加入氢氧化钡溶液至中性可知两者的物质的量之比为2:1,从而化学方程式为:2NaHSO4 +Ba(OH)2=2H2O+BaSO4↓+Na2SO4,故离子方程式为:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D正确.
点评:本题从物质能否拆分、电荷守恒和原电池的反应式等角度考查了离子方程式的书写,难度适中.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
下列有关说法正确的是( )
| A、一定条件下,使用催化剂能加快反应速率但不能改变平衡转化率 |
| B、氢氧燃料电池的能量转换形式仅为化学能转化为电能 |
| C、升高温度水的离子积常数减小 |
| D、根据能量守恒定律,反应物的总能量一定等于生成物的总能量 |
下列说法不正确的是( )
A、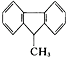 分子中的所有碳原子不可能同时在一个平面内 分子中的所有碳原子不可能同时在一个平面内 |
B、按系统命名法,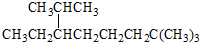 的名称为2,2,7-三甲基-6-乙基辛烷 的名称为2,2,7-三甲基-6-乙基辛烷 |
C、目前市场上大量矿泉水、食用油等产品包装瓶几乎都是用PET(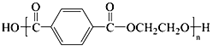 )的合成单体之一是对苯二甲酸 )的合成单体之一是对苯二甲酸 |
| D、有一种信息素的结构简式为CH3(CH2)5CH═CH(CH2)9CHO,为验证该物质中既含有醛基又含有碳碳双键,向该物质的试液中先加过量的溴水溶液,观察到溶液褪色,再向溶液中加入新制的Cu(OH)2悬浊液,加热煮沸,观察到砖红色沉淀 |
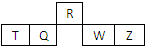 短周期元素R、T、Q、W、Z在元素周期表中的相对位置如下图所示,五种元素中只有一种金属元素.下列判断错误的是( )
短周期元素R、T、Q、W、Z在元素周期表中的相对位置如下图所示,五种元素中只有一种金属元素.下列判断错误的是( )| A、W的单质易溶于CS2 |
| B、Q与R可能形成化合物Q3R4 |
| C、T的最高价氧化物的对应水化物为强碱 |
| D、W、Z都有多种含氧酸 |
下列反应中离子方程式的书写正确的是( )
| A、向Na2CO3溶液中逐滴滴加盐酸:2H++CO32-═CO2↑+H2O |
| B、向FeCl3溶液中通入H2S气体:Fe3++H2S═Fe2++S↓+2H+ |
| C、向碳酸氢钠溶液中滴加过量的澄清石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| D、浓度均为0.1mol/L的硫酸氢铵与氢氧化钠两种溶液等体积混合:NH4++HSO4-+2OH-═SO42-+NH3↑+2H2O |
下列属于物理变化的是( )
| A、氯气溶于水 | B、食物变质 |
| C、石油的蒸馏 | D、光合作用 |
某同学将一小块金属钠投入到硫酸铜溶液中,通过此实验不能证明下列性质中的( )
| A、钠比水轻但比煤油重 |
| B、钠的熔点较低 |
| C、钠与水反应时要放出热量 |
| D、钠与水反应后溶液呈碱性 |